
|
哪些更快“转正”?研究分析102项 FDA 肿瘤药加快批...
2025.07.11
近日,一项发表于JAMA Network Open的研究《FDA 授予加快批准的抗癌药物获得完全批准或撤回所需时间的影响因素》(Factors in Time to Full Approval or Withdrawal for Anticancer Medicines Granted Accelerated Approval by the FDA)剖析了FDA加快批准抗癌药物的...
|

|
七月份 FDA 的6个待批新分子中有5个海外已获批
2025.07.10
外媒Pink Sheet发布了一份7月FDA审批日程分析文章,然而标题里不无遗憾地用了一个新词“American next”(“美国次之”),因为这些审批日程呈现出一个显著现象:大多即将迎来FDA审批节点的新药已在美国海外市场获批。FDA长期以来在新药审批上的先行地位有了明显的松动,这也印证了局长Ma...
|

|
加拿大新指南草案拟放宽生物类似药临床试验要求
2025.07.10
6月,加拿大卫生部(Health Canada,HC)发布了一份新的指南征求意见稿,提出关于生物类似药(Biosimilar)监管政策的重大调整,计划不再强制要求生物类似药制造商开展III期临床试验来证明其产品的安全性和有效性。以往,为了建立生物类似药与加拿大参考生物制品(Canadian Reference Bi...
|

|
欧盟 GMP AI 附录22征求意见,同时修订计算机化系...
2025.07.09
7月7日,欧盟发布了三份GMP文件征求意见稿,分别是《第四章:文件记录》(Chapter 4 Documentation),《附录11:计算机化系统》(Annex 11 Computerised System),和《附录22:人工智能》(Annex 22 Artificial Intelligence),征求意见均截至10月7日。三份指南紧密关联,欧盟从GM...
|

|
BPOG 发布 AI 验证指南,将 AI 生命周期与验证 ...
2025.07.09
7月1日,BioPhorum发布了一份《在受监管的制药环境中实施AI系统》的指南文件,为制药行业在良好生产规范(GxP)环境下应用AI系统提供指导。
随着AI和机器学习(ML)技术在制药行业的广泛应用,药企纷纷接入的同时,AI系统的复杂性和数据驱动特性给传统的计算机系统验证(CSV)带来了...
|

|
国际药政每周概要:EMA 实施新变更框架,FDA 骨髓增...
2025.07.09
【早期开发与临床】
7.2,【FDA】骨髓增生异常综合征:治疗药品和生物制品的开发
【药学研究与CMC】
7.1,【FDA】用于肠外营养的小容量非肠道给药制剂和药房散装包装:铝含量和标签建议
本周BE指南:
【注册与变更】
6.30,【EMA】修订后的变更框架应用指南
【生产...
|

|
邀请药企临床创新,FDA 聚焦贝叶斯、选择性安全数据...
2025.07.08
6月,FDA全面更新了药品评价与研究中心(CDER)临床试验创新中心(CDER Center for Clinical Trial Innovation,C3TI)系列页面,细化了其运行机制,尤其是三大示范项目的参与标准,包括贝叶斯统计分析(BSA),选择性安全数据收集(SSDC)和嵌入临床实践的简化试验(STEP)。申办...
|

|
FDA 与 NIH 合作协调临床和真实世界术语,首批40个...
2025.07.08
FDA与美国国家卫生研究院(NIH)携手开展了一项名为“现代化研究与证据(MoRE)”的跨机构合作项目,并于2023年4月成立了MoRE术语工作小组(MGWG),致力于为与创新性临床研究设计相关的术语制定共识定义,特别是那些涉及真实世界数据(Real-World Data,RWD)的研究。
6月17日,其...
|

|
MHRA 改革临床路径,英国力求生命科学10年后仅次于中...
2025.07.07
6月25日,英国药品和健康产品监管局(MHRA)一口气发布了9份指南文件,配合2026年4月即将实施的新临床试验法规。MHRA称这些新法规是20年来英国临床试验运行框架的最大变化。新法规允许低风险临床试验的申办者在初始申请和后续修改时使用通知方案(notification scheme),将监管和伦理...
|

|
中国香港拟自行审批新药,2026年起分阶段推行
2025.07.07
6月26日,中国香港特区政府卫生署发布新闻稿,宣布香港药物及医疗器械监督管理中心(英文名Center for Medical Products Regulation,CMPR)的成立时间表及推行新药“第一层审批”(Primary Evaluation,中英文翻译沿用原文)路线图。CMPR将于2026年底成立,而卫生署将从2026起分阶...
|

|
国内药政每周导读:医保局促进创新药,电子申报和 eCT...
2025.07.07
【早期开发与临床】
6.30,【CDE】关于再次公开征求《多联疫苗临床研究技术指导原则(征求意见稿)》意见的通知
7.2,【CDE】关于发布《抗 HIV 感染药物临床耐药性研究及数据递交指导原则》的通告(2025年第23号)
【药学研究】
7.1,【CDE】关于公开征求《细胞治疗药...
|

|
【周末杂谈】创新药专利滥用的恶化
2025.07.06
单个药品就可拥有上百项专利的保护,让专利挑战愈加不易
时任FDA代理局长Janet Woodcock医师曾于2021年致函美国专利局Andrew Hirshfeld局长,建议联手遏制专利滥用、鼓励竞争。信中罗列了“专利丛林”、“专利长青”及“产品跳转”等创新药公司常见滥用专利的手段,及FDA对此的关注。 ...
|

|
【轻松一刻】原来我就是质量文化
2025.07.05
识林轻松一刻,意在以漫画形式,展现药企人酸甜苦辣,博得识林读者会心一笑之余,也希望带来些许回味与思索。
识林欢迎读者提供素材,可以是几段对话,也可以是一个故事。有合适的,识林会与您联系,一起优化完善,并由我们的设计师转化为漫画,在识林平台上分享给大家。
识林...
|

|
【招聘】识林求贤 共建药业 AI 应用的新生态
2025.07.05
大语言模型(Deepseek, ChatGPT)为代表的AI工具,为识林十五年来建立的结构化药业知识库融合大语言模型的AI赋能应用带来了潜力。识林正在探索构建“AI赋能 + 知识工程”的企业级AI应用生态,并已有优化效果,提升效率的落地案例:
基于全生命周期、动态更新的权威知识库,支持法...
|

|
EFPIA 调研2024全球官方检查,看 PICS 和各国境外...
2025.07.04
6月10日,欧洲制药工业协会联合会(EFPIA)发布了《2024年度监管 GMP/GDP 检查调查数据》,汇总了27家全球创新型制药企业及两家国家贸易协会提供的数据。
报告显示,全球药品生产监管检查正逐步从疫情期间的远程模式回归传统现场检查,实时远程检查在疫情后逐年减少,但整体检查数...
|
|
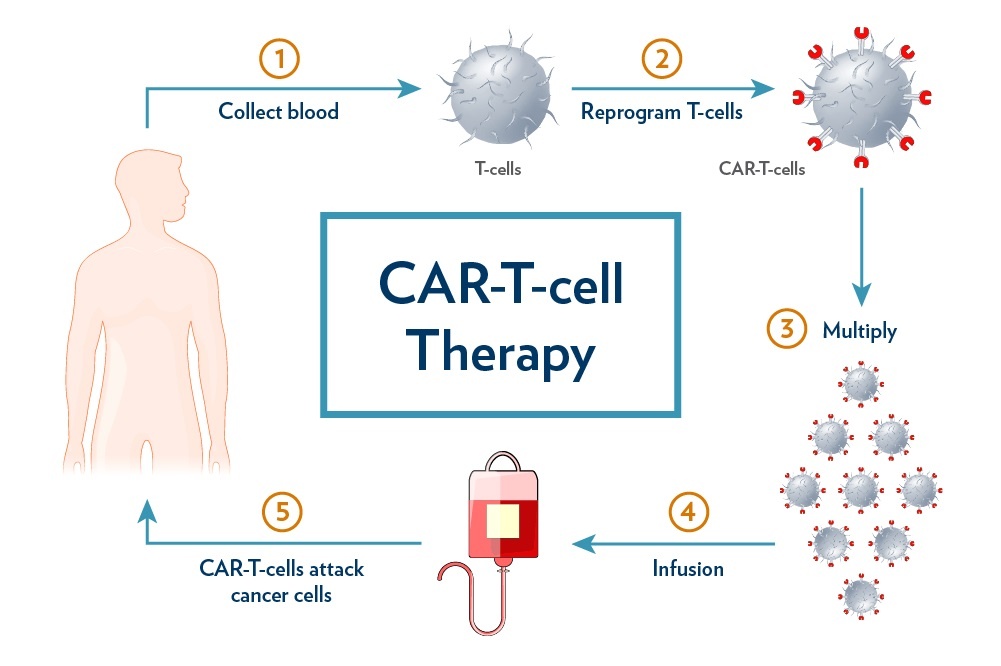
FDA 取消自体 CAR-T 细胞免疫疗法的 REMS 要求
2025.07.04
6月26日,FDA发布安全通讯,取消目前获批的BCMA和CD19靶向自体嵌合抗原受体T细胞(CAR-T)免疫疗法的风险评估与减轻策略(REMS)。
REMS是FDA的一种安全计划。FDA可以要求某些具有严重安全问题的药物实施REMS,以确保药物的获益超过其风险。此前,由于自体CAR-T细胞免疫疗法复杂的...
|

|
FDA 临床药理学办公室2024年报,公开审评总结及大量...
2025.07.03
6月13日,FDA发布了《临床药理学办公室2024年度报告》。该报告详细展示了临床药理学办公室(Office of Clinical Pharmacology,OCP)在过去一年中在药物监管、临床药理学研究以及推动创新药物开发等方面的工作成果与进展。对于我国监管与药企,OCP的大量研究文献具有独特的参考价值。
...
|
|
FDA 肿瘤卓越中心2024年报,丰富工具促进前沿创新
2025.07.03
6月25日,FDA肿瘤卓越中心(Oncology Center of Excellence,OCE)发布2024年报,显示其在肿瘤药品及生物制品的监管审评与推动肿瘤治疗领域发展方面的成果。
OCE监管的肿瘤领域是一直以来的药物开发热点。从其年报即可看出,OCE在曾见证信达礼来PD-1折戟的Pazdur领导下相当活跃,...
|

|
FDA 定稿远程监管评估问答指南,不是检查但需早做准...
2025.07.02
6月26日,FDA定稿了《进行远程监管评估 - 问答》指南,共计16个问答,为制药行业及其他受FDA监管的行业提供关于远程监管评估(Remote Regulatory Assessment,RRA)的明确指导。该指南曾于2022年7月和2024年1月两次征求意见。相比上次征求意见,定稿指南没有显著修订。
RRA是源...
|

|
独立调查报告揭示印度产伪劣抗癌药物被销往全球超百个...
2025.07.02
6月25日,由盖茨基金会资助的独立调查新闻社(The Bureau of Investigative Journalism,TBIJ)发布报告,披露了一起令大众震惊而令研究人员“心碎”(heartbreaking)的全球性药品质量问题。报告显示,多个关键化疗仿制药未能通过质量检测,可能致使全球超100个国家的癌症患者面临...
|