
|
专家点评 USP 1037 过程分析技术草案,比技术更重...
2025.07.21
美国药典(USP)在其药典论坛网站上发布了新的通则草案“过程分析技术:理论与实践”(Process Analytical Technology – Theory and Practice),以及两篇启发性文章(stimuli article)“过程分析技术 I:过程分析技术中的取样理论”和“过程分析技术 II:实时放行检测的实施...
|

|
欧洲药典单抗试点项目收官,更多生物类似药标准在路上
2025.07.21
7月15日,欧洲药品质量管理局(EDQM)发布新闻,欧洲药典委员会(European Pharmacopoeia Commission,EPC)在其第182次会议上正式批准单克隆抗体(monoclonal antibodies,mAbs)试点项目结题。EPC称这标志着在为这类复杂生物治疗药物开发公共标准方面取得了一个重大里程碑,其意义在于...
|

|
国内药政每周导读:注册检验细节优化,制药用水检查,...
2025.07.21
【早期开发与临床】
7.18,【CDE】关于发布《存在未满足临床需求的严重细菌感染性疾病抗菌药物临床试验技术指导原则》的通告(2025年第27号)
【药学研究】
7.14,【NMPA】关于发布仿制药参比制剂目录(第九十四批)及调出参比制剂目录品种清单(第二批)的通告(2025年第26号)
...
|

|
【周末杂谈】药品效期可(应)延长?
2025.07.20
延长效期不仅节省药费,提高便捷性,还可在紧急时期缓解药品短缺
也许是由于曾经缺医少药及国内药房可方便地买到各种各样的非处方药,似乎家家都有存药的习惯。且一存就是几年,常常用时发现已过期了。不禁要问,例如:才过期3个月,还能用吗?
家庭如此,政府也如此。例如,政府需要...
|

|
讲座回顾与问答合集:FDA 近期趋势对中国药业影响
2025.07.19
7月2日,识林如约举办了题为 “FDA 近期趋势对中国药业的影响——人员机构变动、审评模式创新与增加海外飞检” 的线上讲座。本次讲座的背景是FDA近期发生的一系列重大变化,包括加大突击检查力度、加快审评、接入人工智能(AI)以及针对性的政策动向(例如叫停出口细胞用于基因编辑)等等...
|

|
PDUFA VIII 流程启动:降低收费,更加透明?
2025.07.18
FDA与制药行业的处方药使用者付费法案(PDUFA VIII)谈判进程即将启动,在7月14日PDUFA VIII谈判公开启动会上,FDA局长Marty Makary关于降低公司费用的发言引发业界关注,另外,行业代表也提出诸多透明性要求。
现行PDUFA VII协议将于2027年9月30日到期。涵盖2028-2032的PDUFA VI...
|

|
AC 会上,FDA 要求行业代表“克制”自己的法定权利
2025.07.18
FDA在7月9日举行的儿科专家咨询委员会(Pediatric Advisory Committee, PAC)会议上,对非投票行业代表的角色提出明确限制。
FDA局长Marty Makary曾于4月17日发布指令,限制药企等受FDA监管的公司员工担任专家咨询委员会(AC会)正式成员。然而根据1997年《FDA现代化法案》(FDA Moder...
|

|
FDA 局长干预未果,KalVista 口服 HAE 新药 EKTER...
2025.07.17
7月7日,生物制药公司KalVista Pharmaceuticals宣布,FDA批准其新型血浆激肽释放酶抑制剂EKTERLY(sebetralstat),用于治疗遗传性血管性水肿(HAE)成人患者和12岁及以上儿童患者的急性发作。这是首款口服的按需使用的HAE药物。
sebetralstat的批准并不顺利,不仅FDA推迟了其PDUFA...
|

|
韩国药典成为药典讨论组(PDG)候选成员,此前印度已...
2025.07.17
7月14日,韩国药典(Korean Pharmacopoeia)被选定为药典讨论组(Pharmacopeial Discussion Group, PDG)的下一候选成员,正式开启加入该组织的流程。
PDG成立于1989年,由美国、欧洲和日本的药典组织联合组成,旨在协调全球药典相关议题。近年来,该组织开始扩大规模,以进一步...
|
|
EMA 推进临床试验贝叶斯统计应用,平衡效率与严谨
2025.07.16
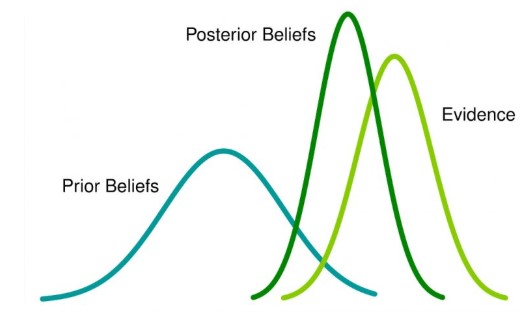
欧洲药品管理局(EMA)即将发布概念性文件,以明确贝叶斯统计在临床试验中的使用规范。此前,EMA于6月17日举办了一场技术研讨会,讨论贝叶斯统计在临床试验中的应用及其潜在优势与挑战。
贝叶斯统计方法允许临床试验申办者在分析中纳入外部信息,从而可能带来诸多潜在效率提升,例如...
|

|
EMA 优先审评 PRIME:门槛较高,且并非总能加快
2025.07.16
基于Pink Sheet数据库,2025年上半年,EMA的优先药物计划(PRIME)共收到23项申请,其中仅8项获得批准,其余15项未能满足EMA严格的资格标准。一如既往,多数申请未能通过。
认定过程相当严格,三分之二被拒
PRIME计划于2016年3月启动,旨在支持和加快未满足医疗需求药物的开发。...
|

|
国际药政每周概要:欧盟 GMP 更新文件记录、计算机...
2025.07.16
【药学研究与CMC】
本周BE指南:
【注册与变更】
7.9,【MHRA】Access,新原料药工作共享计划和生物类似药工作共享计划
7.7,【FDA】MAPP 4191.1 风险评估与减轻策略的修改和校正
7.10,【FDA】FDA 通过公布完全回应函实现彻底的透明性
【生产质量】
7.7,欧盟 ...
|
|
一边短缺,一边获批不上市,行业报告显示美国仿制药市...
2025.07.15
7月10日,IQVIA在其《美国药品短缺和ANDA批准趋势》(Trends in Drug Shortages and ANDA Approvals in the U.S.)报告中指出美国药品短缺的背景却是大量已获批ANDA(简化新药申请,即仿制药申请)未能上市。
美国医疗体系长期面临药品短缺问题,截至2024年6月,FDA报告称有...
|

|
再生元 vs 安进,业界瞩目生物类似药专利博弈
2025.07.15
再生元(Regeneron)与安进(Amgen)之间的专利诉讼引发了制药行业的广泛关注。这场诉讼不仅涉及双方的商业利益,更触及生物类似药市场的发展与专利制度的边界问题。
诉讼涉及再生元眼科“重磅炸弹”Eylea,主要用于治疗湿性年龄相关性黄斑变性等眼疾。Eylea的专利保护期至2027年,其...
|
|
FDA 公开的202份完全回应函“新”在哪儿?
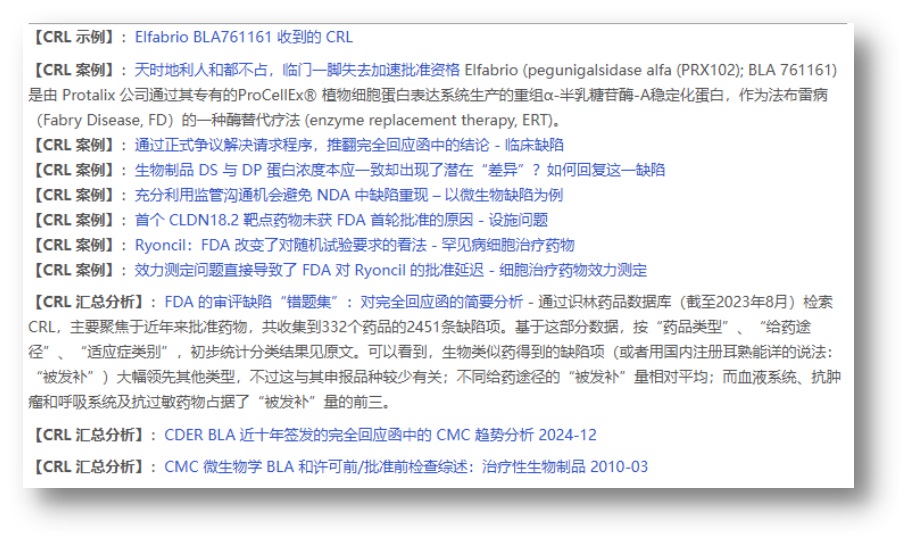
2025.07.14
7月10日,FDA网站发布一则新闻:FDA 通过公布完全回应函实现彻底的透明性(FDA Embraces Radical Transparency by Publishing Complete Response Letters),称当日公开了签发给2020-2024年提交的药品或生物制品上市申请的200多份完全回应函(CRL)文件,给出了第一批CRL的下载链...
|

|
术语、算法和表格模板:FDA 审评新药安全性的工具
2025.07.14
6月,FDA发布了两份政策和程序手册(MAPP),分别为MAPP 6025.8 《审评质量管理规范: OND 定制医学查询》(Good Review Practices OND Custom Medical Queries,OCMQs)和MAPP 6025.9 《审评质量管理规范:标准安全性表与图》(Good Review Practices Standard Safety Tables an...
|

|
国内药政每周导读:附条件批准工作程序再征意见,参比...
2025.07.14
【药学研究】
7.7,【NMPA】关于发布仿制药参比制剂目录(第九十三批)的通告(2025年第24号)
【注册与变更】
7.7,【NMPA】再次公开征求《药品附条件批准上市申请审评审批工作程序(试行)(修订稿征求意见稿)》及政策解读意见
【新药批准和报产】
7.7-7.13,NMPA发布...
|

|
【周末杂谈】又一项事与愿违的政府做法?
2025.07.13
限制创新药和仿制药的专利私了,反而会降低药品可及性
上周提到创新药专利泛滥导致创新药和仿制药专利私了,损害患者利益,促使政府考虑修法来限制私了,仿制药业为此喊冤。实情更为复杂,也更有意思。
1984年建立的《价格竞争与专利补偿法》(俗称《仿制药法》)是通过平衡创新和仿制...
|
|
国产色谱数据管理系统法规符合性专家评审会摘要
2025.07.12
国产色谱数据管理系统如何提供符合国际监管标准的合规保障?为探讨这个国产化替代的核心技术挑战,识林应华谱科仪邀请,与中外监管和行业专家一起,就其自主研发的色谱龙3.0(Chromloong)数据管理系统开展了为期两天的专家评审会。会议摘要供大家参考。
系统架构:合规性源于收费模式设...
|

|
日本 PMDA 发布2024年 GMP 年报,检查中国最多,...
2025.07.11
7月7日,日本药品和医疗器械管理局(PMDA)发布《2024年GMP/GCTP年度报告》。该报告详细总结了PMDA在过去一年中对药品生产质量管理规范(GMP)及基因、细胞和组织产品生产质量管理规范(GCTP)的监管工作成果。报告还随附了一份典型缺陷清单,共计43项缺陷。
目前报告是日文版,PMDA...
|