
|
USP 负责人谈动物试验替代的近期动态
2025.08.05
近日,USP 首席执行官 Ronald T. Piervincenzi 在接受美媒Pink Sheet采访时表示,美国药典(US Pharmacopeia,简称 USP)正在积极寻求动物试验的替代方案,以减少药物生命周期中的动物使用。
Piervincenzi表示,在替代动物试验方面,USP 已取得显著进展。例如,传统的家兔...
|
|
FDA 公开内部文件,为加速批准采取更灵活的药学审评
2025.08.04
8月1日,FDA药品质量办公室(Office of Pharmaceutical Quality,OPQ,负责药学审评)更新内部政策和程序手册《MAPP 5015.13 Rev. 1 加速计划下药品的质量评估 》R1版,并将其从内网转移至公共网络分享。
该文件的发布是为了履行《处方药用户费用法案》(Prescription Drug User F...
|
|
时隔十年,FDA 更新 API 生产检查合规指南
2025.08.04
8月1日,FDA更新合规项目手册《 CPGM 7356.002F 原料药工艺检查》,专门针对原料药(API)生产设施的现场检查,涵盖了对API生产与分销各环节的全面监管,包括生产工艺、质量控制、储存和分发等。该CPGM的上一版本还是10年前。
FDA并不频繁更新CPGM,名义上也是给内部员工参考,但...
|

|
国内药政每周导读:CDE 药物暴露-效应关系,罕见病...
2025.08.04
【早期开发与临床】
7.30,【CDE】关于发布《模型引导的罕见疾病药物研发技术指导原则》的通告(2025年第25号)
7.30,【CDE】关于发布《罕见疾病药物临床药理学研究技术指导原则》的通告(2025年第26号)
7.30,【CDE】关于发布《药物暴露-效应关系研究技术指导原则》的通告(2...
|

|
【周末杂谈】聚焦患者的药品监管,散焦了啥?
2025.08.03
从FDA在罕见病基因治疗上的出尔反尔,看可能的公卫不公
过去两周,FDA有一些不同寻常的举措。当然,这是发生在具体产品监管层面的。宏观政策层面的不同寻常,已见怪不怪了。
7月18日周五,因有患者在治疗中因急性肝损伤而死亡,FDA要求美国Sarepta公司全面停止发放其治疗肌肉萎缩罕见...
|

|
【课程与会议】近期更新的重点课程和8月会议预告
2025.08.02
近期更新重点课程
识林升级版用户,可在PC端和App、小程序移动端学习57个模块的800+门课程6000+节视频,涉及药品研发、注册、生产、质量等全生命周期,包括IPEM项目部分精华课程摘要,监管和学术机构专题教学和研讨会,以及供应商技术介绍专业课程。除视频内搜索、收藏、评论功能外...
|

|
Woodcock 的《质量业务领导力宣言》
2025.08.01
早在2004年,当时从药品评价与研究中心(CDER)主任升任FDA副局长和首席医学官的Janet Woodcock医学博士就勾勒出FDA的愿景:“一个灵活、敏捷的制药制造业,能够可靠地生产高质量的药品,而无需过多的监管。”("A flexible, agile pharmaceutical manufacturing sector that reliably...
|

|
FDA 发文谈制药质量管理的经济价值
2025.08.01
7月28日,FDA发布了一份不同寻常的文件,题为《制药行业的质量管理举措:经济视角》。正当全球药企都在着力应付FDA的检查,甚至部分药企陷入一种“应试”乃至“警察抓小偷”的困局中时,FDA却提醒药企找回质量管理的初心。而且这初心不是道德口号,恰恰是管理层挂在嘴边的“降本增效”。...
|

|
FDA CBER 主任,首席医学和科学官 Prasad 突然离...
2025.07.31
7月29日,美卫生部发言人宣布FDA生物制品评价与研究中心(CBER)主任Vinay Prasad离职,距离其上任不过百日。上一任CBER主任Peter Marks于3月28日被迫离职。
美媒分析此次离职事件部分源于过去一周右翼势力(也是特朗普坚定支持者)对他的强烈反对。此外,Prasad近期要求Sarepta暂...
|

|
白宫发布 AI 行动计划,FDA 可能启动“AI 沙盒”
2025.07.31
7月23日,白宫发布了《美国AI行动计划》(America’s AI Action Plan)。这份计划书脱胎于2025年1月签署的第14179号行政令。该行政令指示联邦政府消除人工智能(AI)创新的障碍并制定国家战略。在经过公开咨询并收到超过1万条建议后,该计划终于发布,内容涵盖了来自行业、学术界和政...
|

|
FDA 针对食品药品的着色剂要求的近期趋势
2025.07.30
作者:识林社区向导@白bai
2025 年2月,特朗普签署法令,建立“让美国再次健康(MAHA)”委员会,其是推动美国医疗保健体系变革的政治和文化倡议,倡导更全面、以患者为中心的医疗模式。卫生与公众服务部(HHS)部长小肯尼迪在公开场合上表示,石油基合成着色剂无营养价值,且与儿...
|

|
GDUFA IV 流程启动,看仿制药企的“愿望清单”
2025.07.30
7月11日,FDA与仿制药行业召开启动会,第四期《仿制药使用者付费法案》(GDUFA IV)的谈判拉开帷幕。双方就复杂仿制药的开发、审批流程的透明度以及与FDA沟通渠道的优化等议题展开讨论。
GDUFA III协议将于2027年9月到期,与处方药和生物类似药使用者付费计划(PDUFA VII和BsUFA I...
|

|
【直播】25年7月全球法规月报划重点
2025.07.30
识林月报直播如期而至,本次直播聚焦7月全球主要监管机构的重点法规,并挑选影响力较大的文件做重点简介。短短40分钟,轻量而轻松,旨在帮助大家回顾上个月的监管重点,加深理解或是查缺补漏。
直播信息速递:
直播时间:8月5日(周二)14点
直播时长:40分钟
直播平台:识林视...
|

|
GSK 的 Blenrep 仍待 FDA 判决,涉及剂量优化和...
2025.07.29
7 月 17 日,FDA肿瘤药物专家咨询委员会(Oncologic Drugs Advisory Committee,ODAC)对葛兰素史克(GSK)的药物 Blenrep(belantamab mafodotin)进行了审查。随后,其7月23日的审评目标日期被推迟至10月23日,同时GSK向FDA提交一份主要补充资料,包含来自DREAMM临床试验的额外数据...
|

|
DMD 药物上市许可被欧盟撤销,但仍在欧洲多国持续销...
2025.07.29
近日外媒报道,PTC Therapeutics的杜氏肌营养不良(Duchenne Muscular Dystrophy,DMD)治疗药物Translarna(ataluren)的欧盟有条件上市许可(Conditional Marketing Authorization,CMA)于2025年3月被正式撤销,但仍在部分欧洲市场持续供应。这一罕见情形引发广泛关注。
Transla...
|

|
国际药政每周概要:FDA 局长优先券启动,EMA 外部对...
2025.07.29
【早期开发与临床】
7.21,【EMA】证明用于哮喘和慢性阻塞性肺病(COPD)的经口吸入制剂(OIP)治疗等效性的要求的指南
7.25,【EMA】关于在监管决策中使用外部对照进行证据生成的思考性文件的制定的概念性文件草案
【药学研究与CMC】
7.21,【EMA】吸入制剂和鼻用制剂药品...
|
|
Nature 子刊发文全景展示我国制药行业创新十年
2025.07.28
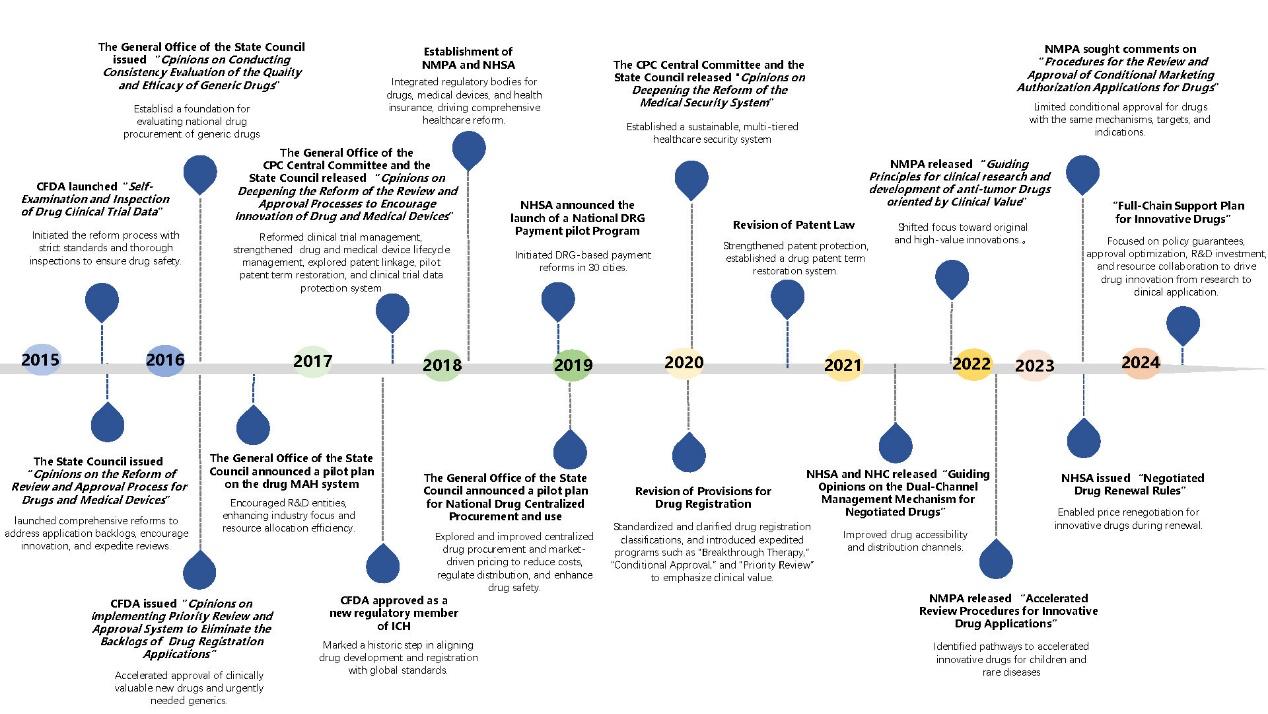
7月21日,正值“7·22”事件十周年之际,《自然综述:药物发现》(Nature Review Drug Discovery)发表了我国监管科学专家、IPEM讲师陈晓媛老师团队的文章《2015–2024中国制药行业崛起:十年创新》(The rise of China’s pharmaceutical industry from 2015–2024 a decade of inn...
|

|
国内药政每周导读:医保称集采不唯低价,CDE 生物类...
2025.07.28
【药学研究】
7.22,【CDE】关于发布《生物类似药药学相似性研究的问题与解答》的通告(2025年第30号)
【注册与变更】
7.22,【CDE】常见一般性技术问题解答 - 新增4个问答
【市场准入与经营】
7.25,【国务院】国家医保局:集采中选不再简单以最低报价作为参考
【...
|

|
IPEM 课程 创新药 IND 药学变更;制药质量体系中...
2025.07.28
化学创新药IND期间的药学变更研究
授课老师:霍秀敏
上课日期:8月22日(周五)
授课方式:中文
上课教室:上海
老师简介
霍秀敏女士,曾任国家药品监督管理局药品审评中心高级审评员、主任药师,主要从事化学药品CMC审评工作。负责参加起草《化学药物质量标准建立的...
|

|
【周末杂谈】合规工作的质量基础
2025.07.27
从一则GMP合规专家的征聘广告,看CMC的重要性
最近看到一则美国著名律所公开招聘GMP合规专家的广告(其中译文附在本文后面),读后有两点感慨。
第一,虽说诚聘专家的主职是GMP合规,但工作内容列表上的前两条,却都是与质量(CMC,Chemistry, Manufacturing 和 Control)相关的,...
|