|
FDA 减免肿瘤生物药动物试验,涉 PD-1 和 ADC ...
2026.06.01
FDA肿瘤学卓越中心(OCE)于5月29日发布指南草案,将动物试验减免措施延伸至肿瘤药领域,针对生物制品和偶联药物提供了简化非临床安全性项目的路径。
FDA建议申办者采用基于风险、产品特异性的非临床开发计划,而非默认开展大量动物毒理研究。内容重点聚焦于3个月毒理研究的减免条件...
|
|
美参议院考虑 ABLA 路径,生物药版 ANDA 在路上
2026.06.01
美国约翰霍普金斯医院医生、医疗保险支付咨询委员会(MedPAC)成员Brian Miller近日在参议院健康、教育、劳工和养老金(HELP)委员会听证会上提议,FDA应建立正式的“简化生物制品许可申请”(ABLA)路径,移除许多现有生物相似性研究要求,以类似小分子仿制药ANDA路径的方式降低生物药...
|

|
国内药政每周导读:eCTD V4.0 指导原则,细胞外囊...
2026.06.01
【非临床和临床研究】
5.27,【海南局】印发《关于支持进口创新药和改良型新药落地转化的若干措施》的通知
5.29,【CDE】关于发布罕见疾病创新药物研发鼓励试点计划(“关爱计划-延伸”)的通知(药审业〔2026〕177号)
5.29,【CDE】关于公开征求《青少年体重管理适应症临床...
|

|
【周末杂谈】公布 CRL,刚开始前途就不保了?
2026.05.31
受保密协议的影响,未来FDA公开未批准上市药品的信息,会变难了
这周三,美国政府《联邦公报》(Federal Register)登出了一项对《联邦雇员保密协议》(草案)(non-disclosure agreement, NDA)征求意见的公告,旨在为所有联邦机构提供统一的保密协议样式,用以确认联邦雇员知悉并...
|

|
【课程与会议】近期更新的重点课程和6-7月会议预告
2026.05.30
近期更新重点课程
识林升级版用户,可在PC端和App、小程序移动端学习57个模块的1000+门课程8000+节视频,涉及药品研发、注册、生产、质量等全生命周期,包括IPEM项目部分精华课程摘要,监管和学术机构专题教学和研讨会,及供应商技术介绍专业课程。除视频内搜索、收藏、评论功能外,...
|

|
【直播】26年5月全球法规月报划重点
2026.05.30
识林2026年5月报直播如期而至,并同步推出5月报。本次直播聚焦5月全球主要监管机构的重点法规,并挑选影响力较大的文件做重点简介。短短40分钟,轻量而轻松,旨在帮助大家回顾上个月的监管重点,加深理解或是查缺补漏。
月报获取渠道:
会员:关注直播当日(6月8日,周一)的【最近更...
|

|
Makary 下台幕后,是 FDA 和行业的双向失序
2026.05.29
近日,Endpoints发布调查报道,基于多个匿名人士信息,披露了几家生物技术公司如何通过秘密游说活动,直接向白宫和国会议员施压,最终推动FDA局长Marty Makary下台。
本文编译自Endpoints的报道原文,目的并非为了讲述大洋彼岸的曲折故事,而是旨在为中国出海药企提供参考,尤其是FD...
|
|
日本 PMDA 单抗毒理简化:6个月试验可减免
2026.05.29
日本药品和医疗器械管理局(PMDA)于5月20日发布《关于单克隆抗体一般毒性评价的考量(早期考虑)》,本文件针对传统单克隆抗体(未修饰免疫球蛋白),阐述PMDA对于一般毒性评价的合理化安排,以及基于新方法学(NAMs)数据的证据权重(WOE)方法的毒性评价思路。
该文件是PMDA推行3R...
|
|
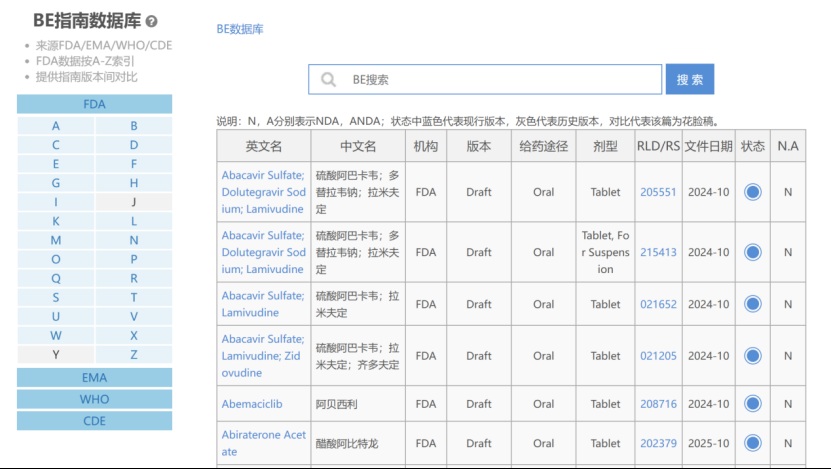
FDA 发布71份 BE 指南,包含多个国内有参比无指南...
2026.05.28
5月21日,FDA 发布了 23 份新的特定产品生物等效性指南(PSG)草案和 48 份修订版 PSG。
据仿制药政策专家Bob Pollock介绍,FDA 自 2010 年起发布 PSG,旨在帮助企业了解其对具体产品BE要求的最新看法,截至 2026 年 3 月已累计发布 2407 份。
新增PSG尽管是草案(d...
|

|
EDQM 强调复溶药品储存风险,建议补足使用中稳定性研...
2026.05.28
5月19日,由欧洲药品质量管理局(EDQM)协调的欧洲委员会药品实践和药学监护质量和安全标准专家委员会(CD-P-PH/PC,“委员会”),发布关于复溶药品储存延期的立场文件。委员会基于调查发现,医院药房对复溶药品设定的使用中储存时间超出产品特性摘要(Summary of Product Characteri...
|

|
加拿大定稿生物类似药指南,非临床和临床均可简化
2026.05.27
加拿大卫生部(HC)于2026年5月19日发布定稿指南《生物类似药的信息和申报要求指南》(此前曾于2025年6月征求意见),明确了与加拿大参照生物制品(Canadian Reference Biologic Drug,CRBD)高度相似的生物类似药的审批路径。
加拿大此次定稿指南延续了国际主流生物类似药监管理...
|

|
FDA 分享3个利用真实世界数据获批的案例
2026.05.27
FDA药品审评与研究中心(CDER)资深流行病学家Motiur Rahman在5月19日的行业监管教育(REdI)会议上展示了三个案例研究,说明申办者如何有效利用真实世界证据(RWE)和真实世界数据(RWD)获得产品批准。
自2016年《21世纪治愈法案》(21st Century Cures Act)要求FDA建立RWD评...
|

|
英国 MHRA 提出罕见病药 IMA 路径,替代传统 IND ...
2026.05.26
英国药品和健康产品管理局(MHRA)5月21日发布罕见病治疗监管框架征求意见稿,提出名为"研究性上市许可“(Investigational Marketing Authorization,IMA)的新路径,旨在将罕见病药物传统10-12年的研发周期进行"有意义的压缩”。
IMA的核心是通过一次许可,将临床试验批准与渐...
|

|
显著疗效抵消数据缺陷:FDA 批准 Zycubo 的权衡
2026.05.26
FDA于1月12日批准Sentynl公司的Zycubo(组氨酸铜,copper histidinate)用于Menkes病治疗。审评卷宗于近期公开。
据PinkSheet对卷宗的分析,这一批准凸显了FDA在超罕见疾病药物审评中的"大疗效原则":当治疗效果足够显著时,可以克服数据质量方面的严重问题。FDA写道,"所观察到...
|

|
国际药政每周概要:FDA 定稿食物效应指南,PMDA 简...
2026.05.26
【非临床与临床研究】
5.20,【FDA】IND 和 NDA 中评估食物对药物的影响 — 临床药理学考虑
5.19,【加拿大HC】生物类似药的信息和申报要求指南
5.20,【PMDA】关于单克隆抗体一般毒性评价的考量(早期考虑)
【药学研究】
5.19,【EDQM】复溶药品使用中储存时间...
|

|
美议员呼吁财政部禁止美国投资中国生物技术
2026.05.25
5月22日,美国众议院中国特别小组委员会主席John Moolenaar致信财政部长Scott Bessent,要求将生物技术纳入COINS法案的禁止投资范围,限制美国资本和知识产权流入中国生物技术领域。
COINS法案(Comprehensive Outbound Investment National Security Act,全面对外投资国家安全法...
|

|
EFPIA 发 GMP 检查年报,全球互认仍待改进
2026.05.25
近日,欧洲制药工业协会联合会(EFPIA)发布报告《2025年度监管 GMP/GDP 检查调查数据》。该调查自2003年启动,核心目的并非分析检查缺陷,而是通过统计数据推动检查依赖(inspection reliance)的落地,使得PIC/S成员资格和双边互认协议(MRA)为药企减轻更多负担。
报告数据来...
|

|
国内药政每周导读:CDE 定稿化学仿制药审评重大缺陷...
2026.05.25
【药学研究】
5.20,【NMPA】关于适用《M13A:口服固体速释制剂的生物等效性》国际人用药品注册技术协调会指导原则的公告(2026年第49号)
【注册与变更】
5.20,【CDE】关于发布《化学仿制药药学研究重大缺陷情形》和《化学仿制药生物等效性研究重大缺陷情形》的通告(2026年...
|

|
【周末杂谈】创新与仿制标签之争的继续
2026.05.24
从美国最高法院"瘦标签"案件的庭审,看知识产权官司的焦点
今年1月,本专栏讨论了一起原研和仿制就"瘦标签"(skinny label)宣传的问题,将官司打到了美国最高法院。4月29日,最高法院庭审,听取了起诉和辩护双方律师的答辩。法官们并未当场投票表决,这可能需要1-3个月的时间。诚...
|

|
从 FDA 首封 AI 相关 GMP 警告信,看药企 AI ...
2026.05.23
2026年4月,FDA发布的一封cGMP警告信引发了全球制药质量与合规领域的广泛关注。这封发给 Purolea Cosmetics Lab 的警告信中,FDA首次在药品GMP警告信中明确指出 “Inappropriate Use of Artificial Intelligence in Pharmaceutical Manufacturing”,即“药品生产中人工智能的不当...
|