
|
欧盟和日本将分享更多检查信息并加强药典合作
2016.10.11
欧洲药品质量管理局(EDQM)于10月3日宣布与日本监管当局达成新的协议,分享与欧洲和日本双方利益相关的原料药(API)生产场地的药品生产质量管理规范(GMP)检查结果的更多信息,以及加强欧洲和日本药典之间的合作。
检查互认协议
9月13日日本厚生劳动省(MHLW)的医药生活卫生局、药...
|
|
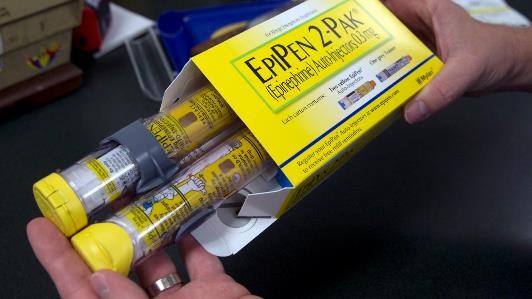
EpiPen价格飞涨V:Mylan就医疗补助退款达成4.65亿美...
2016.10.10
在EpiPen(肾上腺素自助注射器)被报道自1997年底以来在用于低收入者和残疾人的医疗补助计划中一直被错误的归类为仿制药,而被问及有关紧急过敏治疗的医疗补助退款(Medicaid rebates)后不久,Mylan公司没有等待美国司法部(DOJ)对EpiPen的医疗补助(Medicaid)收费开展调查,迅速宣布...
|

|
FDA发布ANDA和505(b)(2)申请最终规定
2016.10.09
FDA于10月6日在联邦公报(FR)公布了一项实施《2003医疗处方药、改善和现代化法案(MMA)》第XI篇的最终规定(Abbreviated New Drug Applications and 505(b)(2) Applications)。FDA自2003年起一直根据MMA第XI篇的法规条款监管,而现在(根据各种法院判决和FDA经验)在法案通过1...
|

|
第二届国际药品连续制造研讨会简报
2016.10.08
2016年9月26-27日,https//iscmp2016.mit.edu/ 第二届国际药品连续制造研讨会在位于美国波士顿旁的麻省理工学院(MIT)举行,全球300余人参会。其中包括来自美国、欧盟和日本的监管部门人员。国内来自北京大学、东富龙和药明康德的代表参会,其中药明康德代表还做了大会报告。会议由诺...
|
|
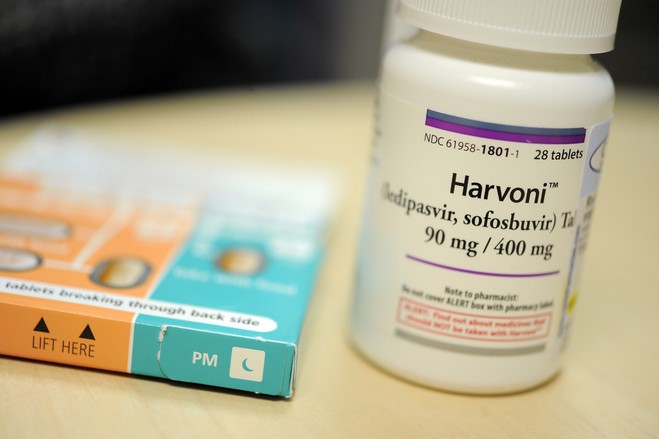
美国$1000一片丙肝药被上黑框警告
2016.10.07
FDA日前发布药品安全公众信,要求9款治疗丙肝的直接作用抗病毒(Direct-acting Antiviral, DAA)药品在标签、说明书、患者用药手册及医师用药指南中,以“黑框警告”的形式明确标明对乙肝复发的风险.
2013年末Gilead推出1,000美元/片的高效抗丙肝药品Sovaldi以来,紧接着推出的Ha...
|

|
FDA发布有关不能配药药品的最终规定
2016.10.07
“FDA正在修订其法规修正已经从市场上撤销或移除的药品清单,因为药品或这些药品的成分被发现是不安全的或无效的(简称“已撤销或已移除清单”或“清单”)(§ 216.24 (21 CFR 216.24))。出现在已撤销或已移除清单上的药品不得根据《联邦食品、药品和化妆品法案》(FD&C法案)503A...
|

|
制药商指责中间商收取回扣,哄抬药品价格
2016.10.06
随着美国药品价格上涨,制药商正努力撇清责任,为制药商在药品价格上涨中所起的作用开脱,取而代之的是,将责任归咎到帮助决定药品定价的中间商。
最为尖锐的一些批评指责,来自于因为药品问题一直受到立法机构严厉质问和社交媒体抨击的一些制药行业高管。包括制造救命药EpiPen自助注...
|
|
FDA具体产品生物等效性指南修订后的思考
2016.10.05
10月4日美国FDA发布67份具体产品生物等效性(BE)指南,其中34份新增33份修订,这是今年第三次批量发布和更新BE指南。FDA一直忙于放出新的BE指南和修订过去的指南文件。根据GDUFA II的新规定,仿制药办公室(OGD)将设定目标在最早合法批准日期至少两年之前针对90%的产品发布具体产品BE...
|
|
医保目录与基本药物小考
2016.10.05
十一假期之前,有如下两则新闻引起行业关注
(1)人力社保部发布2016年国家基本医疗保险、工伤保险和生育保险药品目录调整工作方案征求意见稿
(2)全国药政工作座谈会近日在山东省济南市召开,探讨进一步巩固完善基本药物制度
医保报销对企业推广产品的帮助无需多言...
|

|
WHO预认证项目新收费结构每年将增加2千万美元收入
2016.10.04
世界卫生组织(WHO)于9月30日公布针对其药品和疫苗预认证项目(PQP)的新收费框架,会产生大约2千万美元的年收入(约为预认证项目运营成本的一半),以帮助确保项目长远的财务稳定,并将项目的产品范围扩展到包含治疗诸如癌症和糖尿病等疾病的产品。
根据新收费框架,按照国家监管机构...
|

|
FDA发布指南草案澄清对风险评估与减轻策略的判定
2016.10.03
美国FDA于9月20日发布的《法定因素在判定REMS必要性时的应用》指南草案,试图进一步解释其风险评估与减轻策略(REMS)监管模式的应用,澄清FDA对于《联邦食品、药品和化妆品法案》(FD&C法案)505-1部分(21USC 355-1)所规定的判定REMS是否是必要的因素的应用。
REMS继2007年9月FDA...
|

|
【更新提示】药政信息摘要2016.09
2016.09.30
主题词更新推送 IND、参比制剂、生物标志物、细胞治疗(细胞免疫治疗)
药品数据管理规范(征求意见稿)(09.30)
关于征求《新药I期临床试验申请技术指南(草案)》意见的通知(09.30)
《药品上市许可持有人制度试点方案》政策解读(二)(09.30)
企业参...
|
|
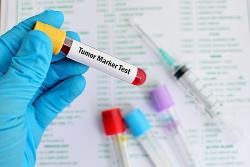
FDA就生物标志物用作临床结果的举例清单征询评议
2016.09.29
美国FDA正就在新药研发中用作临床结果(outcomes)的生物标志物(biomarkers)举例清单征询利益攸关方的意见。(https//www.federalregister.gov/documents/2016/09/19/2016-22470/a-list-of-biomarkers-used-as-outcomes-in-development-of-fda-approved-new-molecular-ent...
|

|
美国会延长儿科优先审评券计划并扩大适用资格
2016.09.28
9月27日美国众议院继参议院之后一致通过决定将罕见儿科疾病优先审评券(PRV)计划(下简称为“儿科PRV计划”)延长至2016年12月31日,目前议案已呈交给奥巴马总统正待签署。宾西法尼亚州民主党参议员Bob Casey的发言人表示,从现在到12月30日期间,国会将讨论如何修订计划并再次延长。
...
|

|
FDA拒绝AbbVie关于美国宪法第五修正案征用的请愿
2016.09.27
9月23日FDA在批准Amgen公司的Amjevita(adalimumab -atto)的同时,正式拒绝的许可将构成根据美国宪法第五修正案(Fifth Amendment)要求公正赔偿的征用(taking)。毕竟,那些参照产品申办人没有在适用法律和FDA在BPCIA之前时代的声明的基础上合理地预期其BLA中包含的商业秘密和机密信...
|

|
辉瑞宣布放弃公司拆分计划
2016.09.26
辉瑞公司于9月26日表示将保持一个公司,决定放弃把公司一分为二的构想(一块专注专利保护药品,另一块专注现金充裕的老产品)。这一决定意味着这家总部位于纽约的制药公司仍将是行业规模最大的公司之一。预计公司今年至少有510亿美元的收入,来自于不断增长的抗癌和疫苗系列产品以及昂贵的...
|
|
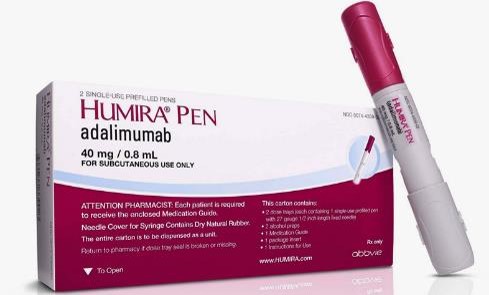
阿达木单抗生物类似药Amjevita获FDA批准
2016.09.25
美国FDA于9月23日批准Amgen公司的Amjevita(adalimumab -atto)作为AbbVie公司Humira(阿达木单抗)的生物类似药用于治疗多种炎症性疾病,成为第四个获得FDA批准的生物类似药。Amjevita被批准适用于参照产品标签上的7种适应症,但没有获批用于另外四种受孤儿药产品专营权保护的适应症,...
|

|
GDUFA II期关键条款一瞥(二)
2016.09.24
相关阅读:【GDUFA II期谈判完成,关键条款一瞥 - 识林资讯 2016/9/5】
美国仿制药使用者付费计划(GDUFA) II期谈判已经完成,那么GDUFA II期中到底都有些什么呢?9月23日联邦公报(FR)上公布了一则关于GDUFA II期公开会议的通告,通告本身提供了对于GDUFA II期变化的一些...
|

|
FDA发布仿制药场地自我认定指南
2016.09.23
美国FDA于9月22日发布《仿制药设施、场地和机构的自我认定》定稿指南。根据2012仿制药使用者付费修正案(GDUFA),所有仿制药设施、场地和机构必须遵循GDUFA的自我认定要求。该指南文件旨在帮助企业理解自我认定要求,从而使得自我认定更容易实现。文件还讨论了哪些设施、场地和/或机构需...
|
|
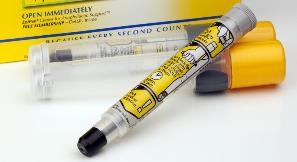
EpiPen价格飞涨IV:仿制药注射器装置问题
2016.09.22
美国FDA药品审评和研究中心主任Janet Woodcock在9月21日举行的听证会上,对参议员概述了确保注射器装置问题可能需要的一些步骤(例如,确保给药的正确剂量)已经得到了解决。虽然她没有提到任何可能受到影响的潜在申办人,Woodcock表示Teva制药和Sanofi也许能够使用这一过程来帮助他们的...
|