
|
【更新提示】识林一周回顾(20190728-0803)
2019.08.04
【FDA】指南草案 罕见儿科疾病优先审评凭证(07.30)
儿科罕见病优先审评凭证计划是旨在促进某些严重和危及生命的罕见儿科疾病的药物和生物制剂开发的一项计划。根据该计划,获得针对罕见儿科疾病的药物或生物制品批准的制药公司可能有资格获得可兑换的凭证,以接收对不同产品的上市的...
|

|
FDA公布处方药、生物类似药、动物药2020财年费率
2019.08.03
前不久美国 FDA 公布了 2020 财年仿制药使用者付费(GDUFA II)的费率标准,识林专文对比了费率方面的变化【FDA公布2020财年GDUFA费率,项目费大幅下降 2019/07/27】。现在 FDA 相继公布了另外一些使用者付费计划 2020 财年费率,我们简要查看一下各个计划的费率情况。
处...
|

|
印度药业反击质量问题指责,兰伯西揭发者尖锐回应
2019.08.02
关于印度制药业数据可靠性和质量管理的问题,我们经常看到的是监管机构的视角,现在我们换个角度,从当事人的视角来看看,本文摘选整理了印度 Biocon 药业掌门人 Kiran Mazumdar Shaw 发表在印度媒体上的公开言论,以及原兰伯西(Ranbaxy)高级管理层、Ranbaxy 案件的揭发者 Dinesh ...
|

|
FDA撤销厂房设施信息递交指南,为什么?
2019.07.31
监管政策制定是政府、企业和社会共同探索的过程,这一过程向全社会的公平、公开、透明是确保制定出行之有效的政策的基础。
美国 FDA 于 7 月 22 日宣布撤销其在 2016 年 12 月 28 日发布的《以电子格式提供监管信息 — 制造设施信息的递交》(Providing Regulatory Submissions in ...
|

|
FDA 谈如何避免数据可靠性问题影响药品批准
2019.07.30
当美国 FDA 了解到其批准了基于可疑生产数据的药品时,后果可能会很严重,但如果公司保持冷静并采取 FDA 介绍的一些关键步骤,则结果可能会大不相同。
FDA 药品质量办公室工艺与设施办公室主管 Derek Smith 最近在加州圣地亚哥举行的药物信息协会(DIA)年会上的演讲概述这种情...
|

|
美国行业协会关于专利滥用阻止生物类似药竞争的分析
2019.07.29
美国普享药协会(AAM,原仿制药协会)生物类似药委员会于 6 月 25 日发布了一份关于专利滥用阻止生物类似药上市销售的白皮书,分析了获得 FDA 批准而未能上市的 8 个生物类似药,得出由于专利滥用导致生物类似药延迟上市而给医疗保健系统带来的损失达 76 亿美元。同时提出了促...
|

|
【更新提示】识林一周回顾(20190721-0727)
2019.07.28
【案例】FDA VMF 申报流程图
【案例】FDA VMF 申报流程材料清单(07.24)
本周,识林整理了VMF申报流程图和材料清单,在材料清单中,详细介绍美国市场的三类MF,Type II VMF的适用范围等背景知识,并且VMF申报流程中的关键步骤,例如创建ESS和ESG账户,自我认定,厂址注册和产...
|

|
FDA公布2020财年GDUFA费率,项目费大幅下降
2019.07.27
美国 FDA 于 7 月 26 日宣布了 GDUFA II 期第三个年头 — 2020 财年(2019 年 10 月 1 日起至 2020 年 9 月 30 日止) 的费率,大多数收费类别均有所下降,其中项目费降幅最大,下降了近 11%,相当于为大公司节省了二十万美元。
另外,由于 FDA 在设定 20...
|

|
行业对 ICH Q12 五味杂陈,部分企业已制定实施计划
2019.07.26
虽然工业界对于 ICH Q12 指南是否会放松批准后变更程序持怀疑态度,但这并没有阻止业界为今年晚些时候可能发布并施行的定稿指南做好准备。一个好消息是,美国 FDA 保证,对于旧有产品,制药商将不需要生成太多新数据来证明 ICH Q12 下批准后变更的合理性。相反,他们应该能够利用...
|

|
FDA 代理局长谈未来工作重点
2019.07.25
美国 FDA 代理局长 Norman Sharpless 在 7 月 23 日发给全体工作人员的题为“现代化工作框架以提高患者和消费者获益”的备忘录邮件中阐述了四项主要工作重点,希望在其剩下的短暂代理局长期间产生重大影响,包括:通过新兴技术保障公众健康,投资 FDA 下一代专家工作人员和基础...
|

|
口服固体缓控释制剂专题青岛会议(第三轮通知)
2019.07.24
高端制剂暑期论坛
口服固体缓控释制剂专题青岛会议
第三轮通知
2019年8月3 - 4日
青岛海泉湾皇冠假日度假酒店
主办单位:北京大学药物信息与工程研究中心
承办单位:青岛百洋制药有限公司
支持单位:上海安必生制药技术有限公司;北京宽见科技有限公司
...
|

|
当 CMO 收到警告信时,你该怎么办?
2019.07.24
当你作为一家制药商,寻找到一个合适 CMO,并且完成了前期的调查、审计、技术转移、变更申报等一系列准备工作,就要开始生产或者已经开始生产了,此时你的合同商收到了警告信,你会如何反应,又该怎么办?
背景
你作为药品上市申请的持有人,刚刚对你所拥有的商业销售药品完成了向...
|

|
ICH Q12 将于年底发布,FDA 已启动审评员培训
2019.07.23
ICH Q12 《药品生命周期管理的技术和监管注意事项》指南预计将于 11 月获得最终批准,将克服与欧盟不同立法体系的冲突,并更为清晰地阐明既定条件(established condition)相关内容。另外,FDA 正针对 Q12 的一些关键原则对员工进行培训,以确保审评的一致性。
7 月 15 日在美国...
|
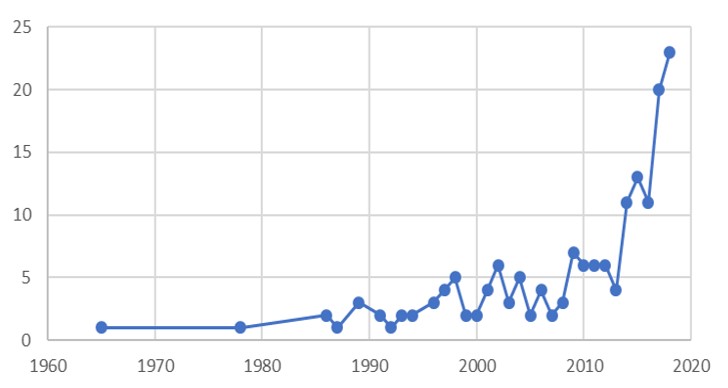
|
从 FDA 批准数据看生物药发展趋势
2019.07.22
2019 年已经过半,我们趁现在来找个机会看看 FDA 和行业在生物药申请批准方面做的如何,同时将这类产品的批准情况放入历史的长河中看看有着怎样的趋势和变化。
从 1965 年到 2013 财年结束,FDA 批准了大约 86 个治疗性生物制品(TBP)。早期,批准率非常缓慢,前 22 年间仅有...
|

|
【更新提示】识林一周回顾(20190714-0720)
2019.07.21
【国务院】印发《关于建立职业化专业化药品检查员队伍的意见》
【国务院】关于建立职业化专业化药品检查员队伍的意见(07.19)
7月18日,国务院办公厅印发《关于建立职业化专业化药品检查员队伍的意见》。在主要目标中指出到2020年底,国务院药品监管部门和省级药品监管部门基本完...
|

|
FDA 最终决策多大程度上会听从咨询委员会建议?
2019.07.20
随着美国 FDA 正在努力应对越来越大的新药批准压力,最近发表的一项新的研究发现,仅在较少情况下,FDA 的行动会与咨询委员会的建议出现分歧,并且与批准新产品或现有产品的新用途相比,在药品安全问题上更容易出现分歧。
根据1972年联邦咨询委员会法(FACA)实施的咨询委员会(Advisory...
|
|
FDA在废品场发现GMP文件,印度药厂再陷数据可靠性漩涡
2019.07.19
美国公众与监管机构对于在亚洲生产的药品质量一直不能放心,最近一封涉及美国仿制药最大供应商之一 — Strides 药业的警告信再次说明了问题的严重性。
根据 FDA 本周在其网站上发布的 7 月 1 日的一封警告信,FDA 检查员在位于印度 Puducherry 的 Strides 工厂的废品场发...
|

|
英国医学杂志刊文:多数新药无新益,监管审批过宽
2019.07.18
德国卫生技术评价机构最近发表在《英国医学杂志》(BMJ)上的一篇分析发现,大多数新批准的药实际上与标准治疗没有太大区别,并呼吁对药物开发和批准进行国际化政策改革。
德国医疗质量与效率研究所(IQWiG)审查了 2011 年至 2017 年间的 216 个新批准 — 152 个新分子实体和 ...
|

|
维护(Maintenance)4.0:如何着手
2019.07.17
上次我们在【维护(Maintenance)4.0 – 制药行业的下一次革命 2019/06/28】中介绍了维护4.0的核心方面,并概述了全面的维护流程。在本文中,我们将讨论如何着手开展维护4.0,以及如何制定基准指标,以评估当前和期望状态之间的差距。
维护4.0不会改变使资产处于可靠、合规、...
|

|
FDA 将改进辅料数据库以包含最大每日暴露量数据
2019.07.16
美国 FDA 于 7 月 10 日发布《辅料数据库的使用》指南草案,解释了即将对 FDA 的辅料数据库(IID)开展的一些改进,包括将增加每种辅料的最大每日暴露量(maximum daily exposure,MDE)以及对数据库更频繁地更新。指南还介绍了如何使用 IID 及其局限性。
指南表示,“将根据GD...
|