|
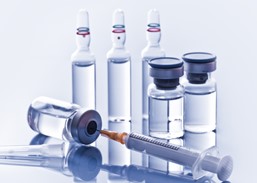
无菌生产的持续风险 - 诺和诺德欧洲工厂483分析
2016.02.28
不像固体口服制剂药品那样不需要灭菌,肠道外药品必须被灭菌,并且由于其性质,许多肠道外药品不能终端灭菌。在无菌工艺中,药品和包装容器首先需要分别灭菌,然后再放在一起。鉴于这种情况,无法在最终容器中对药品灭菌,最终产品必须在一个极其高质量的环境中灌装和密封。参见FDA行业指...
|

|
FDA新任局长致全体员工的信
2016.02.27
编者按:FDA新任局长在信中表示“我未来最重要的工作重点是支持和加强FDA卓越的员工团队,从而使我们可以继续保持我们的能力跟上迅速变化的世界。”FDA已经是公认的世界上最卓越的团队,还在继续加强并且是局长最重要的工作,把发展最快的生命科学的研究和公共卫生产品结合在一起,持续...
|

|
仿制药办公室主任提供GDUFA实施进展更新
2016.02.27
FDA仿制药办公室(OGD)主任Kathleen “Cook” Uhl医师在GPhA年会上提供了OGD在实施GDUFA I方面的进展更新。尽管在她的报告之前的专家小组会指出了OGD的“紧张”和不确定性,Cook给出了强有力的信息,OGD到现在为止已经满足所有GDUFA目标,并且已经超出了GDUFA目标函中所列的目标。
自从...
|

|
FDA仿制药办公室与企业的紧张关系仍待改善
2016.02.26
Scott Gottlieb医师在GPhA年会闭幕日仿制药办公室(OGD)主任Uhl医师报告OGD的更新之前,举行了一个三人专家会。Scott向Kate Beardsley(Beardsley律师事务所)、Sheldon Bradshaw(FDA前首席律师,Hunton和Williams律师事务所合伙人)和Frances Zipp(Lachman Consultants总裁兼CEO...
|

|
Me-Too药物的回归?大企业的2016年获批期望集中在熟...
2016.02.26
2015日历年中,FDA药品研究与审评中心(CDER)批准了45个新药,这些新药是新分子实体(NME)或新的治疗用生物制品。其中有21个罕见病用药;16个first in class;但是常见疾病的me-too药品比较少,详见2015年FDA CDER新药审批总结。制药业跟随监管机构的激励,创造了破纪录的新药批准数...
|

|
参议院确认Califf为新任FDA局长
2016.02.25
本周三(2月24日)美国参议院议员以压倒性多数投票(89-4)确认Robert Califf为FDA新任局长。
FDA代理局长Stephen Ostroff医师在FDA网站上发表声明表示“Califf医师通过他在科学和医学领域作为医师、研究人员和领导者的杰出职业生涯证明了推进公共卫生的长期而深刻的承诺。他清楚地明白...
|

|
GDUFA II期谈判和FDA行动趋势
2016.02.23
GDUFA II期谈判正在紧锣密鼓的进行。与小企业相关的付费问题是正在讨论的话题之一,尤其是设施费问题是否仅应该在ANDA批准后收取。这也是国会关注的问题,并将在谈判讨论中获得显著关注。公开地谈判会议纪要还解决了像申请审评的GDUFA目标日期、补充申请时间和来自企业回复的增补审评时间...
|

|
北京大学连续制造研讨会-第三轮通知
2016.02.22
转载自:北京大学药物信息与工程研究中心 www.cpier.pku.edu.cn
北京大学连续制造研讨会
第三轮通知
北京大学中关新园1号楼,科学报告厅
中国,北京 2016年3月9-10日
目的
讨论制药生产创新方面的最新发展,包括连续制造
联合主要学术、产业和监管利益攸关方
...
|

|
定期安全性更新报告(PSUR)自今年6月起统一向EMA提交
2016.02.21
自2016年6月13日起,欧洲企业将不再向国家监管机构提交定期安全性更新报告(PSUR),而是向欧洲药品管理局(EMA)的中央资料库(Repository)提交。PSUR资料库根据2012年7月通过的立法建立,并提供了相关评估报告、额外数据和评议的存储。
英国监管机构在https//www.gov.uk/guidance/pe...
|

|
FDA因潜在药品短缺豁免海正进口禁令中的盐酸柔红霉素
2016.02.19
2月18日美国FDA表示因潜在短缺问题将允许来自浙江海正药业的一种化疗用原料药盐酸柔红霉素的进口。
2015年3月2-7日,FDA在对海正台州原料药生产基地现场检查时发现严重的GMP违规,核心是数据可靠性问题,见检查结束时留下的483缺陷表。2015年9月9日FDA发布了针对该基地的进口禁令(impor...
|
|
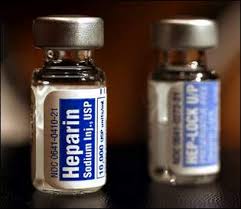
FDA低分子量肝素表征和免疫原性考量指南定稿
2016.02.19
2月18日,FDA发布题为《低分子量肝素(LMWH)免疫原性相关考量》的最终更新指南。指南对(ANDA中)活性成分一致性的正确表征以及此类产品的免疫原性检测考量提供了建议。该指南为NDA持有人(新产品或已有产品的变更)和ANDA申请人提供指导。关于变更的建议适用于原始申请,以及原材料或其...
|

|
用数字解读FDA的第II类DMF完整性审查
2016.02.18
一、FDA网站公开的DMF数量
从2012年10月1日GDUFA实施以来,正式提出了仿制药原料药的完整性审查(completeness assessment,CA)。原料药DMF被 2012 年 10 月 1 日后提交的ANDA, ANDA Amendment 或ANDA PAS首次援引时,需要一次性缴付 DMF 费,每年缴付场地费。原料药DMF持有...
|

|
Sandoz就商业上市通知问题提请最高法院审查
2016.02.17
Sandoz提请最高法院审查联邦巡回上诉法院关于BPCIA 商业上市前180天通知规定的裁决
商业上市前通知在FDA批准前提交是否有效,以及在任何情况下作为独立的要求并给予所有生物类似药在批准后延迟180天上市的禁制令是否是不适当的。这是Sandoz在本周早些时候(向最高法院提请上诉的截止之...
|

|
FDA加速审批药品的上市后安全监管数据有待加强
2016.02.16
上个月,美国审计总署(GAO)公开发布关于FDA处理药品上市后安全监管的报告调查结果,GAP是向国会提供审计、评估和调查服务的独立的无党派机构。报告的标题为《FDA加速许多申请的审评,但批准后监管数据亟待加强》)更快进入市场的药品的安全性。GAO报告受国会议员康涅狄格州民主党人Rosa ...
|
|
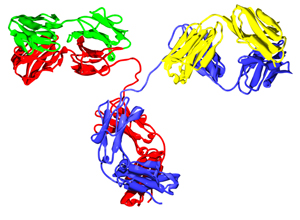
英利昔单抗生物类似药获专家会审通过,适应症外推引争...
2016.02.15
美国FDA顾问委员会以压倒性的多数投票支持韩国的Celltrion公司和辉瑞公司对强生旗下Janssen公司Remicade的生物类似药的许可,为美国首个单克隆抗体生物类似药的推出开辟了道路。
2月9日,FDA关节炎顾问委员会以21-3投票支持生物类似药CT-P13适用于与杨森公司的参照生物制品Remicade(...
|

|
美国FDA前局长陷入联邦诉讼
2016.02.14
FDA前局长Margaret Hamburg医师,被指控涉嫌合谋隐瞒强生公司抗生素Levaquin(左氧氟沙星)有害影响的有关信息,与此同时她的丈夫经营从强生公司股票获利的对冲基金。
事件概览
Margaret Hamburg在辞去FDA局长职务近一年之后,正面临一名保守派、激进主义分子、政府监督律师提起的...
|

|
FDA发布第II类API DMF完整性评估指南终稿
2016.02.13
2月12日FDA发布行业指南终稿《GDUFA下第II类API DMF完整性评估》,旨在帮助正在或将要在简化新药申请(ANDA)、ANDA的增补、ANDA的之前已获批申请的补充申请(PAS)或PAS的增补(仿制药提交)中首次被引用的第II类原料药(API)药物主文件(DMFs)的持有人应对DMF的完整性评估。(注:第I...
|

|
美国阿片类药物滥用流行点评
2016.02.11
在美国,阿片类药物滥用导致的死亡人数一直在迅速上升。2014年阿片类药物导致了惊人的28,648人死亡,超过了道路交通事故死亡人数。阿片类滥用现在是美国年轻人最大的单一杀手,虽然各年龄组均受到阿片滥用的影响。阿片类药物引起的死亡迅速上升,并影响美国农村和城市各地,已成为一个全...
|

|
2016年FDA指南文件计划的更多点评
2016.02.11
1月26日我们曾发布资讯关于FDA药品审评和研究中心(CDER)公布的将于2016年新起草和修订指南的日程计划,并挑选了一些指南稍作评论【识林资讯-2016年FDA计划新起草和修订指南日程】。下面我们挑选了今年可以期待的另外一些指南稍加点评,按分类列举如下:(完整的文件清单请见此处)
...
|

|
2017财年FDA申请51亿美元财政预算
2016.02.10
FDA新闻稿 url=http//www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm485144.htm?source=govdelivery&utm_medium=email&utm_source=govdelivery
2016年2月9日
FDA正在申请51亿美元的总预算作为总统2017财年预算的一部分用于保障和促进公众健康,比2016...
|