|
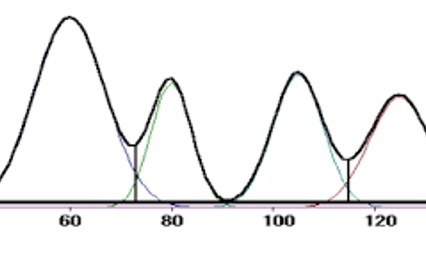
WHO 良好色谱实践亮点分析
2019.02.27
2月21日,WHO发布了良好色谱实践(Good Chromatography Practices)征求意见稿文件,这是非常有意义的、专门适用于色谱的良好实践。为更好的理解该文件,我们收集了安捷伦公司专家对于文件的点评,并在此基础上对于文件的特色部分做了亮点分析。
安捷伦大中华区液相产品应用经理陈波...
|

|
FDA 发布 22 篇新 BE 指南和 52 篇修订指南
2019.02.26
美国 FDA 于 2 月 22 日发布了一批 74 篇具体产品生物等效性(BE)指南,其中 22 篇新增,52 篇修订。
这些指南中针对复杂药品的有 4 篇新增指南和 45 篇修订指南,其中包括 16 种目前尚无仿制药获批的产品。总共有 35 篇指南是针对尚无获批仿制药的产品。另外,有 ...
|

|
从免费到 37 万美元的孤儿药故事后续:参议员质询与...
2019.02.25
不久前我们曾发文报道了一则怪事,FDA 批准了一个新药,却使得市场上原本治疗相同疾病免费的药物直升到每年 37 万美元【刚发生的孤儿药定价奇闻:从免费到年价37万美元】。这个新药就是 Catalyst 公司的 Firdapse,FDA 批准的首个用于治疗 Lambert-Eaton 肌无力综合症(LEMS)的药。自 ...
|

|
【更新提示】识林一周回顾(20190217-0223)
2019.02.24
【IPEM】3月课程通知(02.17)
3月7-8日,由Aloka Srinivasan 博士主讲原料药注册申报与评审,课程内容包括FDA有关API的指南文件;如何编写高质量的DMF;如何理解FDA关于API的提问并做出合适的回复等。3月9-10日肖柏明 博士主讲药物质量分析,指导怎样学习 ICH Q 系列指导原则;IC...
|
|
FDA 再生医学疗法加快程序定稿指南解读
2019.02.23
美国 FDA 于 2 月 15 日发布《适用于严重疾病的再生医学疗法的加快程序》定稿指南,澄清了在临床试验中可能会考虑历史对照,申办人可以为一个给定产品请求并获得一个以上的加快程序认定,以及对于产品的生产变更不一定会阻碍最初的再生医学先进疗法(RMAT)认定或导致 RMAT 认定被...
|
|
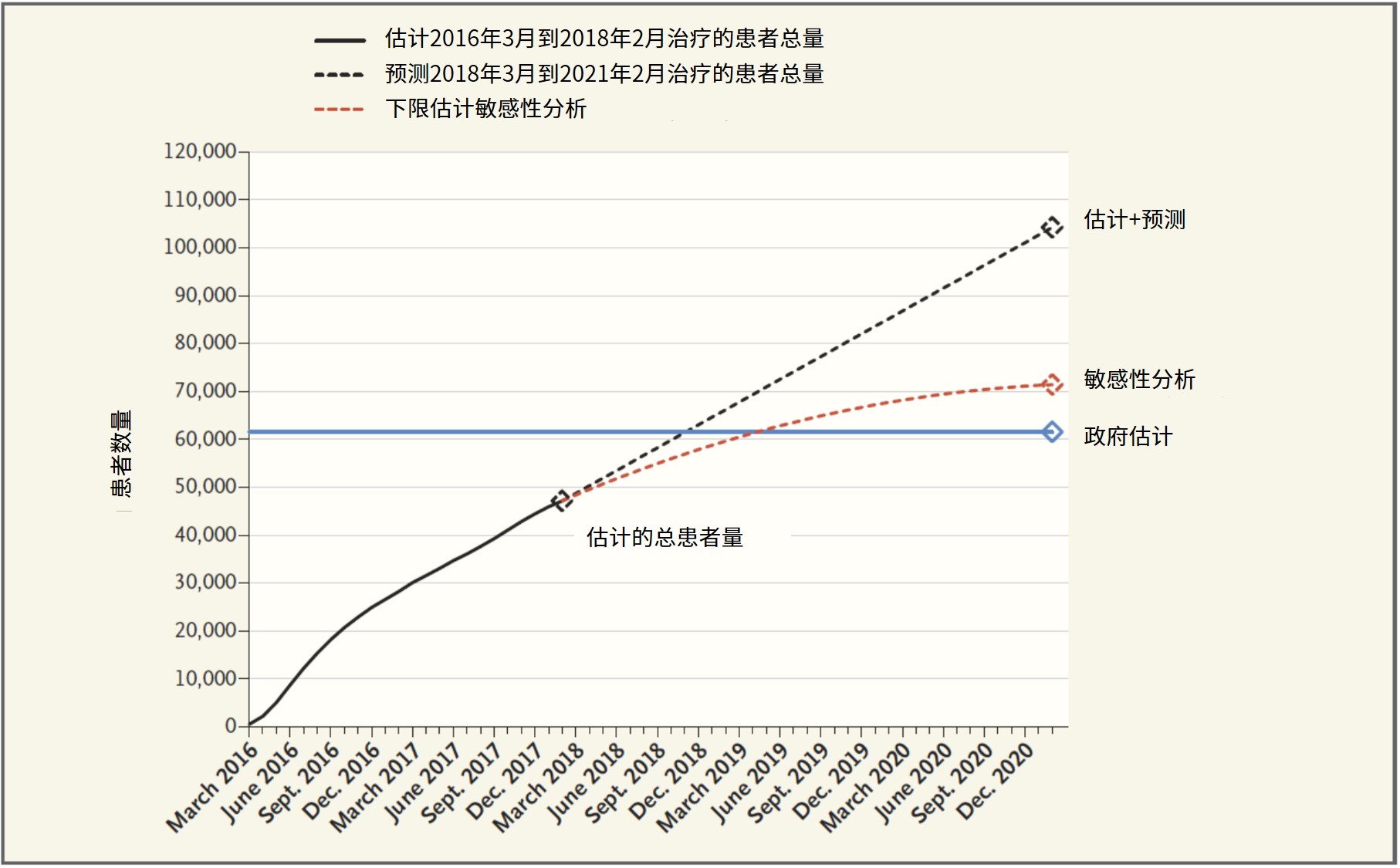
澳大利亚政府采用丙肝药品预约订购模式节约大量资金
2019.02.22
澳大利亚的丙肝治疗药品预约订购模式(Netflix 模式)预计将使患者成本降低约 85%。近期在《新英格兰医学杂志》上发表的一篇文章分析了澳大利亚政府于 2015 年通过谈判达成的一项协议:在 5 年内花费约 7.66 亿美元以换取供应商提供无限量的丙型肝炎(HCV)直接作用的抗病毒药物...
|

|
FDA 2019 财年拨款获十年来最大幅度增长
2019.02.21
美国 2019 财年度综合拨款法案终于在经历了许多不确定性和拖延之后获得总统签署成为法律。作为最终财政支出计划的一部分,FDA 2019 财年获得的拨款比去年增加了近 2.69 亿美元,实现了十年间年度预算的最大增长。
更强 FDA 联盟(Alliance for a Stronger FDA)的 Steven Gro...
|

|
FDA 对于复杂仿制药与原研药的标签差异把控或有松缓...
2019.02.20
美国 FDA 于 1 月 30 日批准的重磅哮喘治疗吸入器的仿制产品 — Mylan 公司 Wixela Inhub(丙酸氟替卡松/沙美特罗)的患者使用说明明显不同于参照产品 GSK 公司的 Advair Diskus(舒利迭),反映了 FDA 在复杂仿制药方面愿意接受某些器械设计和标签的差异。【Advair 吸...
|

|
FDA 启动有关药品质量的“既定条件”试点计划
2019.02.19
美国 FDA 于 2 月 14 日宣布了一项新的试点计划,以测试在药品申请质量评估中的“既定条件(Established Conditions,EC)”概念。该试点的目的是让 FDA 在评估拟议既定条件方面获得实践经验,并确保评估决策不会对使用者付费时间框架产生负面影响。EC 是“为保证获批产品的工艺...
|

|
FDA 发布竞争性仿制药指南草案
2019.02.18
美国 FDA 于 2 月 15 日发布《竞争性仿制药》指南草案,介绍了 2017 年《FDA 再授权法案》(FDARA)第 506H 条的新法定要求。竞争性仿制药(CGT)的颁布是为了促进和激励研发,加快对某些仅有很少或没有竞争的已获批药品的仿制药的审批。此外,在某些情况下,这些法律条款的激...
|

|
【更新提示】识林一周回顾(20190210-0216)
2019.02.17
【IPEM】2019年IPEM课程教育3月份即将开班(02.13)
3月在北京大学中关新园开班的首次课由三个课程组成:3月7-8日是Aloka Srinivasan博士的原料药注册申报与审评,重点讲解原料药相关的FDA指南文件,如何编写高质量的原料药DMF文件等内容,该课程适合从事注册、工艺和处方开发和管理、Q...
|

|
FDA 将开展药品质量共识标准的认可计划
2019.02.16
美国 FDA 于 2 月 13 日发布《CDER 与药品质量相关的自愿共识标准的认可计划》指南草案。该计划将允许制药商证明向 FDA 提交的药品申请符合某些共识质量标准。FDA 表示该计划将提高药品质量,鼓励新兴技术的开发并确保更顺畅的药品审评。
该指南介绍了 FDA 药品审评与研究中心...
|

|
FDA 宣布启动供应链安全试点计划并向大型供货商开刀
2019.02.15
美国 FDA 于 2 月 7 日宣布接受来自制药行业及其供应链合作伙伴的申请参与供应链安全试点计划,以测试用于在整个供应链中追溯跟踪处方药的产品标识符、条形码和互操作系统的使用。
《药品供应链安全法案》(DSCSA)于 2013 年 11 月 27 日签署成为法律,概述了构建可以识别...
|

|
FDA 仿制药办公室迎来新主任
2019.02.14
美国时间2月12日,FDA宣布了Sally Choe博士接替Kathleen (Cook) Uhl医学博士(也可译为医师)出任仿制药办公室(Office of Generic Drugs)的新主任。此宣布尚未公布,细节尚不知。
Choe博士现任FDA药品审评和研究中心(CDER)转化科学办公室(Office of Translational Scien...
|

|
FDA 着手整治对膳食补充剂的监管
2019.02.13
2 月 11 日美国 FDA 发布 12 封警告信和 5 封在线告知信*,对 17 家非法销售声称治疗阿尔茨海默等严重疾病的公司采取行动。此次警告的超过 58 种非法销售的产品中许多是作为膳食补充剂在网站或社交媒体平台上出售的,未经 FDA 审查并且未被证明能够安全有效地治疗宣称的疾病。...
|

|
用数据说话:美国仿制药行业现状与挑战
2019.02.12
昨天的资讯“2019 美国仿制药年会简报”中概述了美国卫生与人类服务部(HHS)部长 Alex Azar在仿制药协会年会上的讲话重点。他的演讲内容当然非常精彩充实,但他作为首位在仿制药年会上演讲的卫生部长则具有极大的象征意义。再加上 Azar 在讲话中提到前几天在白宫圆桌会议上特朗普总...
|

|
2019 美国仿制药年会简报
2019.02.11
2019 年美国普享药协会(AAM,原仿制药协会)年会于 2 月 5 日至 6 日在新奥尔良召开,此次的年会主题为“Access!”,聚焦仿制药可及性。下面我们从对会议内容的简报中看看有哪些热点讨论,以及这些讨论对于我国药业有着怎样的参考价值。
会议第一天的议程涉及仿制药和生物类似...
|

|
【更新提示】识林一周回顾(20190203-0209)
2019.02.10
【EMA】发布痛风药物临床研究指南草案(02.08)
本指南提供了关于痛风治疗药物评价的指南,包括预防和治疗急性关节炎发作或慢性痛风性痛风性关节病。潜在的治疗方法可能是降尿酸治疗或抗炎药物。在主要开发用于治疗急性疼痛的产品的情况和研究计划中将急性痛风性关节炎发作作为急性伤害...
|

|
FDA 发布组合产品上市前路径原则指南草案
2019.02.09
美国 FDA 于 2 月 5 日发布《组合产品上市前路径原则》指南草案,提供了 FDA 关于组合产品上市前审评原则的当前考量,包括指导申请人针对自身产品应选择哪种上市前提交类型。指南提供了与组合产品相关的一般性、高层级的信息。
FDA 发布该指南草案是作为实施《21 世纪医药法...
|

|
ICH 正式发文计划协调仿制药标准
2019.02.08
ICH 于 2 月 6 日发布了一份思考性文件(reflection paper),概述了关于跨国协调仿制药技术和科学标准的思考。
该文件建议对非复杂制剂和复杂制剂制定一系列证明生物等效性标准的 ICH 指南。文件还介绍了将于 2019 年组建的非正式仿制药讨论组(Informal Generic drug Discussion...
|