|
总结经验教训,推动持续发展—FDA质量管理成熟度试点...
2023.02.01
2020 年 10 月至 2022 年 3 月,FDA药品审评和研究中心 (CDER) 完成了两项试点计划,以评估药品生产企业的质量管理成熟度 (QMM)。成熟的质量体系促进了对漏洞的主动检测,防患于未然,并培养了一种奖励流程和系统改进的文化。CDER QMM 计划有助于提高供应链的弹性和稳健性...
|

|
加速审批改革:FDA 似不会严格执行加速批准之前完成...
2023.02.01
美国 FDA 药品审评与研究中心(CDER)首席副主任日前在一次会议上介绍了 FDA 计划如何行使新法案赋予的对加速审批路径监督的额外权力。
美国国会于去年年底通过的政府综合拨款法案授权 FDA 加强对加速审批药物的监管,FDA 将有权制定了加速审批药物确证性试验的设计,并可能会要...
|

|
国际药政每周概要:欧盟疫苗临床评估指南,生物类似药...
2023.01.31
【注册、审评、审批】
01.29【EMA】关于支持欧盟生物类似药可互换性的科学依据的声明的问答
【创新研发与临床】
01.27【EMA】EMA 为学术和非营利的先进疗法(ATMP)开发人员提供增强的支持试点的问答
01.27【EMA】疫苗临床评估指南
【GxP 与检查】
【安全性】
【CMC与...
|

|
ECA污染控制策略模板(示例)更新
2023.01.31
2022年12月,欧洲合规学会(ECA)发布了题为“How to Develop and Document a Contamination Control Strategy 2.0《如何制定和记录污染控制策略 2.0版》”的文件,2.0版本也同时更新了附件。这份文件首次发布于2022年2月,基于2020版欧盟无菌附录征求意见稿制定,随后ECA根...
|

|
立法之后坚定推行,美国版“医保国谈”发布工作时间表
2023.01.30
1月11日,美国卫生部下属医保服务中心(CMS)发布备忘录,向公众公开国家医保Medicare药价谈判计划的工作路线和时间表。
去年(2022年)8月,拜登总统正式签署《通胀削减法案》(IRA 2022),自此,在各个利益集团历经多年的反复博弈之后,美国版的“医保国谈”终于以法律的形式落地。...
|

|
美国 FDA 加入国际合作调查受污染的止咳糖浆来源
2023.01.30
美国 FDA 于 1 月 25 日表示,正在与世界卫生组织(WHO)和一些外国监管机构合作,支持对已导致非洲和亚洲 300 多名儿童死亡的受污染止咳糖浆的来源进行调查。
FDA 在一份声明中表示,没有迹象表明受污染的糖浆已进入美国药品供应链,但正在“调查这种危害对 FDA 监管产...
|

|
周末杂谈:FDA好心做好事,但被判违法(续)
2023.01.29
从FDA对法院判决的反应上,看原研药和仿制药的利益之争
本月23日,FDA在美国联邦公告上发布了一项关于罕见病孤儿药的审批政策,声明接受联邦上诉法院对具体案件的判定,但不接受判定对法律条文的一般解释。看待此案件有多个视角,从立法到司法,从企业到政府,从产业政策到公共卫生,各...
|

|
轻松一刻 - 三思而后学?
2023.01.28
识林祝大家开工大吉,让我们新的一年,撸起袖子干中学!
识林轻松一刻,意在以漫画形式,展现药企人酸甜苦辣,博得识林读者会心一笑之余,也希望带来些许回味与思索。
识林欢迎读者提供素材,可以是几段对话,也可以是一个故事。有合适的,识林会与您联系,一起优化完善,...
|

|
ICH Q9(R1) 质量风险管理修订指南正式定稿
2023.01.27
ICH 于 1 月 20 日发布了其Q9《质量风险管理》修订版定稿指南,旨在通过建立更客观的风险评估来改进当前的质量风险管理(QRM)计划,这可能会减少质量缺陷和药品短缺。
修订指南更新了已有 18 年历史的原始指南,涵盖了 QRM 的原则、一般 QRM 流程、风险管理方法、QRM 与行...
|

|
FDA 发布 36 页长 483 报告详述印度工厂数据可靠...
2023.01.26
美国 FDA 最近在一份签发给印度 Intas 药业的 483中严肃谴责该药厂因一系列质量控制缺陷而导致“一连串失败”。
根据 FDA 于 1 月 18 日公布了去年 11 月底在检查了位于印度古吉拉特邦 Intas 工厂之后发出的长达 36 页的 483 报告,Intas 药业多次违反 GMP,存在的问...
|
|
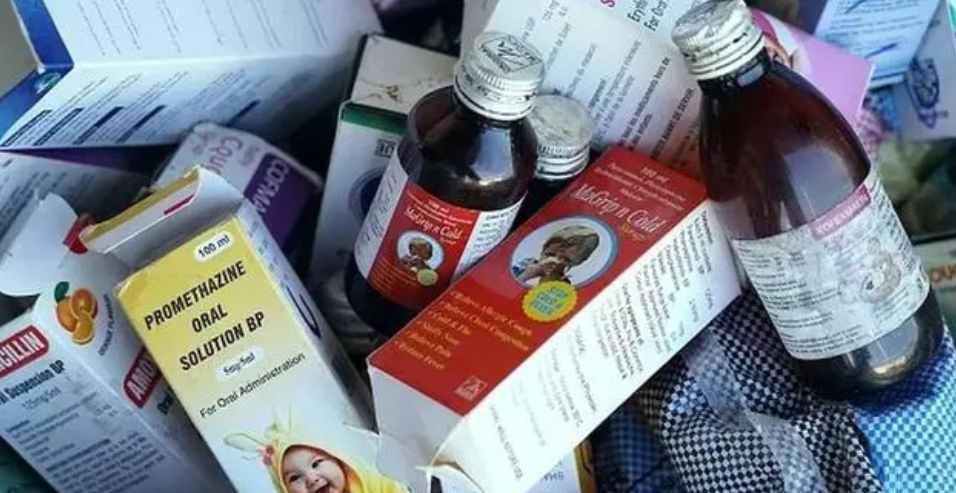
WHO 敦促各国制药商和监管机构对受污染止咳糖浆采取...
2023.01.25
在对受污染的止咳糖浆发布多次警报之后,世界卫生组织(WHO)于 1 月 23 日发布通告,呼吁各国采取紧急行动,以预防、发现和应对伪劣医药产品事件。
WHO 表示,在过去四个月中,各国报告了多起儿童使用的非处方止咳糖浆确认或疑似被高浓度二甘醇(DEG)和乙二醇(EG)污染的事件。...
|

|
国际药政每周概要:ICH Q9(R1)质量风险管理定稿,FD...
2023.01.24
【注册、审评、审批】
【创新研发与临床】
01.17【FDA】指南草案 优化用于治疗肿瘤的人用处方药和生物制品的剂量
01.17【FDA】指南定稿 临床研究者行政行为 - 资质撤销,机构审查委员会、临床研究者和申办方指南
【GxP 与检查】
【安全性】
【CMC与仿制药】
01.2...
|

|
国内药政每周导读:GLP认证管理办法,器械2022审评工...
2023.01.23
【创新药与临床开发】
1.19,【CDE】关于发布《慢性淋巴细胞白血病新药临床研发技术指导原则》的通告(2023年第1号)
【CMC与仿制药】
1.16,【药典会】新增2篇辅料相关标准草案、14篇药包材标准草案的公示
【注册、审评、审批】
1.16,【NMPA】修订3个通用名多个品规的说明...
|

|
【周末杂谈】向大家恭贺新年!
2023.01.22
...
|

|
美众议员致信 FDA 和 NIH 质疑对临床试验结果公开...
2023.01.20
美国众议院能源和商业委员会副主席 Frank Pallone 于 1 月 19 日致信 FDA 局长 Robert Califf 和美国国立卫生院(NIH)代理主任 Lawrence Tabak 表达了对医药产品申办人不遵守向 ClinicalTrials.gov 数据库报告临床试验结果信息要求的担忧。
美国联邦法律要求某些临床试验申办人向...
|
|
美国政府调查报告:改变危险病原体的研究应得到更好地...
2023.01.20
美国政府问责办公室(GAO)于 1 月 18 日发布了一份报告称,卫生部门对可能增强危险病原体研究的监督模糊,缺乏透明度,并且“不完全符合有效监督的关键要素。”
美国国立卫生研究院(NIH)有一个生物安全顾问委员会,预计将在 1 月 27 日的会议上讨论机构对此类研究的监督...
|
|
莫德纳呼吸道合胞病毒(RSV)疫苗3期试验成功,RSV ...
2023.01.19
莫德纳(Moderna)公司于 1 月 17 日表示,其针对呼吸道合胞病毒(RSV)的疫苗在 3 期试验中降低了 60 岁以上人群的下呼吸道疾病发病率。
目前已有三家公司在 RSV 疫苗方面取得进展,除莫德纳之外,辉瑞和葛兰素史克(GSK)已经公布了他们的 RSV 疫苗在老年人身上的结果,...
|
|
FDA 发布抗肿瘤药剂量优化指南草案
2023.01.19
美国 FDA 于 1 月 17 日发布了一份题为“优化用于治疗肿瘤的人用处方药和生物制品的剂量”的行业指南草案,帮助申办人在临床开发中确定抗肿瘤药物的最佳剂量。
从历史上看,抗肿瘤药物的剂量探索试验(包括剂量递增和剂量扩展部分的试验,主要目的是选择推荐的 II 期剂量)一般...
|
|
欧盟正就诺华基因治疗药 Zolgensma 潜在肝损伤问题...
2023.01.18
欧洲药品管理局(EMA)在俄罗斯和哈萨克斯坦两名接受 Zolgensma 治疗的儿童死亡五个月后,正在为医疗保健提供者制定新建议。
EMA 在 1 月 12 日药物警戒风险评估委员会会议之后发表声明称:医疗保健专业人员应及时评估肝功能测试以及/或者急性肝病体征或症状的患者。如果患者对...
|

|
印度产止咳药接连陷入二甘醇污染丑闻,Ranbaxy 揭发...
2023.01.18
受乙二醇和二甘醇污染的由印度 Marion Biotech 生产的止咳糖浆去年 12 月在乌兹别克斯坦再次造成至少 19 名儿童死亡。去年夏天,冈比亚就至少有 70 名儿童在服用印度 Maiden 药业生产受污染咳嗽药后死于肾衰竭。
就在冈比亚事件公开的几天之前,一本由 Dinesh S. Thakur 和 Pras...
|