
|
综合审评:FDA 新药上市申请审评现代化
2021.01.08
最近来自 FDA 新药办公室的科学家们在《治疗创新和监管科学》杂志上发表了一篇文章1,详细介绍了美国 FDA 近几年开展的新药综合审评计划。识林过去曾陆续报道过相关的内容,批评声占多数,比如:【不再透明?FDA不顾反对力求减少审评报告公开信息 2019/09/27】。今天我们通过这篇文...
|

|
科学家批评印度在缺乏有效性数据的情况下匆忙批准新冠...
2021.01.08
《科学》(Science)杂志网站近日发文指出,印度药品监管机构在没有等待确定的有效性和安全性 III 期试验结果的情况下,于 1 月 3 日授权了印度 Bharat Biotech 公司开发的新冠(COVID-19)疫苗 Covaxin,这一行动引发了一些科学家和患者倡导组织的严厉批评。
在周日的新闻...
|
|
醋酸格拉替雷是不是生物产品?法院判决告诉你
2021.01.07
醋酸格拉替雷 (Glatiramer acetate ,GA) 是由四种氨基酸 (谷氨酸、赖氨酸、丙氨酸和酪氨酸) 组成的肽段共聚物混合物。以商品名 Copaxone™上市的醋酸格拉替雷,是 Teva 公司开发的最畅销的多发性硬化症药物,年销售额 40 到 50 亿美元。那么这个药是否应该划为生物产品?T...
|

|
美国卫生部撤销 FDA 关于非处方药专论收费的通知
2021.01.07
美国卫生与公共服务部(HHS)1 月 6 日在联邦公报(FR)上发布了一份不同寻常的通知。
原因是 FDA 缺乏发布该通知的授权权限(FDA lacked the delegated authority to issue the Notice)。卫生部进一步通告表示,已命令 FDA 停止与非处方药专论使用费(OMUFA)计划有关...
|

|
欧盟 2021 年基因疗法申报和批准展望
2021.01.06
全球首次批准的基因治疗药物在 2020 年相对较低,但根据对预期上市许可申请申报和批准决定的分析,这一治疗领域在欧盟市场的活动在 2021 年可能会大大增加。今年可能会有至少五种基因疗法在欧盟首次批准,以及至少三种基因疗法提交监管申报(见文末表格)。
2020 年,由于新冠(COVI...
|

|
辉瑞计划加快向试验安慰剂组受试者提供新冠疫苗接种
2021.01.06
辉瑞及其合作伙伴 BioNTech 计划在 3 月 1 日之前为临床试验中接受安慰剂的志愿者提供新冠(COVID-19)疫苗,这比起最初计划的时间提早了几个月时间。
这项决定代表了美国FDA、辉瑞和疫苗志愿者以及开发另一 mRNA 疫苗的 Moderna 公司之间复杂的公开博弈。FDA 及其专家顾问...
|

|
2021 年值得关注的三大制药行业趋势
2021.01.05
过去的一年着实令人难忘,对于制药行业来说,2020 年也是整个医药产业风口浪尖上的一年。在药价问题使制药业成为众所攻击的靶子后,新冠疫情则让行业成为拯救世界的希望。但是疫情虽然使关于利润、创新和知识产权以及可负担性和可及性的辩论大为缓解,但对于行业来说,这一话题在 2021 ...
|
|
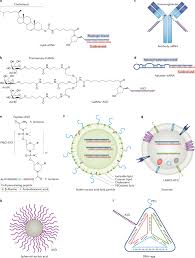
FDA 发布个体化反义寡核苷酸药物申报的指南草案
2021.01.05
2021 年 1 月 4 日,新年的第一个工作日,美国 FDA 发布了一份新的关于个体化反义寡核苷酸药物研究用新药(IND)申请的程序建议指南,提供了有关早期开发和 IND 提交过程的清晰信息,是 FDA 与正在开发这些个体化药物产品的人员合作的第一步。
科学知识和药物开发技术的进步...
|

|
【一周回顾】2020.12.28-2021.01.03
2021.01.04
国家局附条件批准国药集团北京生物制品研究所新冠灭活疫苗。刑法修正案颁布,8条内容与医药领域紧密相关。药审中心节前发布一大批指导原则。WHO 紧急使用认证首个新冠疫苗。FDA 批准胰高血糖素首仿药。英国紧急批准阿斯利康新冠疫苗。
上周热点资讯:
FDA 批准首款合成肽胰高血糖...
|
|
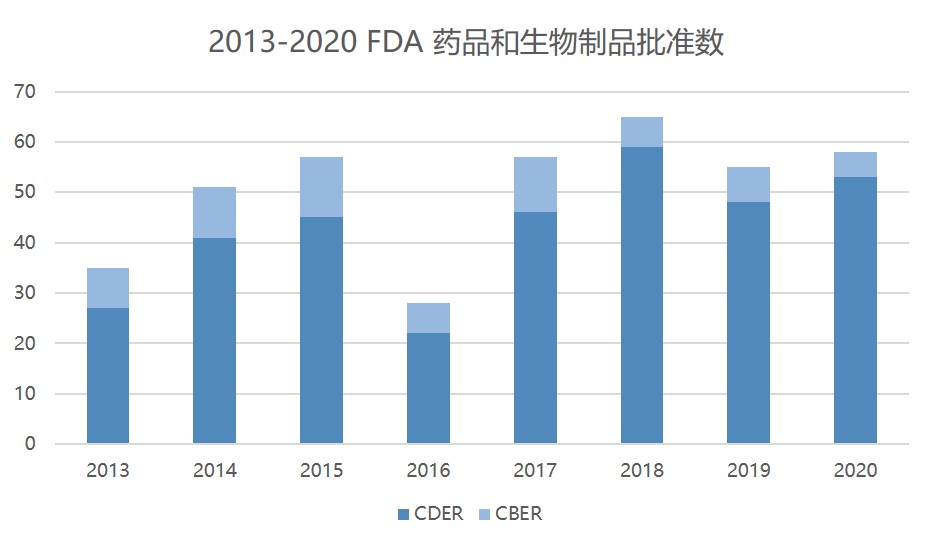
FDA 2020 年药品和医疗器械重点工作回顾
2021.01.04
美国 FDA 在 2020 年总共批准了 50 多个新药,即使是在没有新冠(COVID-19)疫情的年份也是一份卓有成效的成绩单。批准总数不仅超过了 2019 年(48 个新药)的成绩,也是 FDA 自 2018 年(59 个)以来第二次超过 50 个新药批准。
2020 年,药品审评与研究中心(CDE...
|

|
【周末杂谈】啥也不能耽误涨价
2021.01.03
匪夷所思的市场经济和创新生态
太阳从东边升起,人有生老病死,这是一定要发生的事。可以再加一条,药品年年涨价。
可不,1月1日,正当大家过年放假之时,美国70余家药企宣布数百种药品的价格平均上涨3.3%。别急,这只是每年两次涨价中的一次,下半年还涨一次。好日子怎能一下子都...
|
|
辉瑞新冠疫苗首获 WHO 紧急使用,英国和印度先后授...
2021.01.02
世界卫生组织(WHO)于 12 月 31 日宣布将 COMIRNATY® COVID-19 mRNA 疫苗列入紧急使用清单(Emergency Use Listing,EUL),这使得辉瑞/BioNTech 的疫苗成为自新冠(COVID-19)爆发一年以来首个获得 WHO 紧急认证的疫苗。
WHO EUL 为各国加快进口和管理疫苗的监管审批...
|
|
识林资讯的定位
2020.12.31
识林资讯历来重点报道美国FDA的药品监管、及直接和间接相关的时讯。在国际关系复杂化和双循环发展格局的新时期,识林资讯将会一如既往。想法如下。
监管的关键是平衡公共健康和产业发展的需求。全球只有美国和中国(日本和印度在其后),既有规模纵横的药业又有巨大的药品市场。例如,...
|
|
FDA 批准首款合成肽胰高血糖素仿制药
2020.12.30
美国 FDA 于 12 月 28 日批准了美国美药星(Amphastar)公司的首款仿制注射用胰高血糖素 USP 1mg/瓶(急救药盒),用于治疗可能发生于糖尿病患者的严重低血糖症(极低血糖)。该药还可在当需要减少肠蠕动时,在胃、十二指肠、小肠和结肠的放射学检查中作为诊断辅助药物。
FDA...
|

|
FDA 公布 2021 财年非处方药专论企业付费费率
2020.12.30
美国 FDA 于 12 月 29 日公布了非处方药(OTC)专论使用者付费法案(OMUFA)的收费结构和费率。这是 FDA OTC 监管大改革的一部分。【FDA OTC 大改革:收费,18个月专营权,按新药重新提交 2020/05/15】
根据2020 年 3 月 27 日颁布的《冠状病毒援助、救助和经济安全法案...
|

|
2021 年医疗科技行业的三大关键问题
2020.12.29
一年又一年,2020 年注定是非同寻常的一年,在医疗科技领域也是如此。新冠(COVID-19)疫情引发了人们对数字医疗的更多关注,并且带来了创纪录的资金注入。医生们正在使用人工智能驱动的预测工具来标记患者的死亡时刻。借助远程医疗,患者正在接受针对慢性疾病和急症的护理。医学研究参...
|

|
英国药监局公布创新许可途径以加快药品开发
2020.12.29
英国药品与医疗保健产品监管机构(MHRA)发布了有关正在建立的创新许可和获取途径(ILAP)的指南,以加快产品上市时间。这一途径下的药品开发商将收到从 MHRA 及利益相关方(包括英国国家卫生与临床优化研究所)的更多反馈。
药物开发者只要拥有关于新化学实体、生物医学、新适应症或...
|

|
【一周回顾】2020.12.21-12.27
2020.12.28
市场监督总局发布生物制品批签发管理办法;药审中心发布化学仿制药透皮贴剂药学研究技术指导原则;核查中心首次开展进口药品远程非现场检查试点工作。识林上线 FDA 生物制品法规框架与合规优先事项讲座视频。欧盟附条件批准首个新冠疫苗。WHO 发布利福平和利福喷丁中亚硝胺杂质的影响...
|

|
2020 年度生物制药产业的 11 个趋势
2020.12.28
在过去十多年中,一些影响生物加工和生物制药生产的趋势已有所显现,其中大部分有望带来积极成果。而 COVID-19 则加速了许多持续发展的趋势,而且可能会导致永久性变化。
在 BioPlan Associates 今年发布的《第 17 届生物加工行业年度调查与回顾》报告1中,确定了 2020 年十...
|

|
【质量对话】质量,疫情间被遗忘的角落?
2020.12.27
辉瑞和Moderna新冠疫苗,FDA都没有做批准前检查
编辑:据美国媒体报道,获得FDA紧急使用授权的辉瑞-BioNTech疫苗和Moderna疫苗,FDA都没有做批准前检查。这似乎有些不同寻常,也许这是特事特办?
刺槐:问得好,咱们就来讨论一下这两个“特”字。
编辑:我认为,在疫情严重影响...
|