
|
FDA 新任局长工作重点:反击错误信息,加固科学基础
2022.02.21
新上任的美国 FDA 局长 Robert Califf 在 2022 年 2 月 17 日与 FDA 工作人员和公众的首份备忘录中承诺,打击有关科学和 FDA 的错误信息和应对持续的新冠(COVID-19)大流行是其重新掌舵 FDA 后的首要任务。
Califf 于 2 月 15 日以 5046 票的微弱优势得以再次出任...
|

|
【周末杂谈】信达PD1审批与“知己知彼”
2022.02.20
从厂家和客户关系的角度,分析企业与FDA的交流
药品是商品。商品有客户。商品的设计和研发应围绕客户需求。
药品是特殊商品。药品的首客户是药监局。药监局不满意,何谈其他(医生、患者、医保)?
2月10日的“信达”PD1审批专家会上(严格讲,这不是关注疗效的传统意义上的新药...
|

|
讲座:美国律师谈 FDA 关于仅中国试验策略、数据可...
2022.02.18
美国 FDA 官员最近发表了几项声明,重点关注仅在中国进行的成功临床试验可能不足以获得美国批准,更倾向于进行国际多中心临床试验(MRCT)。他们还关注到数据可靠性的重要性,当中国申办人设计旨在获得美国批准的临床试验时来自 FDA 的具体产品建议可能会有帮助,以及在没有事先咨询 F...
|

|
FDA 发布 42 篇 BE 指南,新增诺西那生钠指南
2022.02.18
美国 FDA 于 2022 年 2 月 17 日发布了新一批 42 篇具体产品指南(PSG),为仿制药的开发和生成支持简化新药申请(ANDA)批准所需的证据提供建议,从而帮助简化企业仿制药开发和 FDA 的 ANDA 审评。
这一批 42 篇具体产品指南包括:29 篇新增和 13 篇修订。34 篇(其...
|

|
英国 MHRA 总结新冠疫情期间临床试验经验
2022.02.17
英国药品与医疗保健产品监管机构(MHRA)在其官方博客中回顾了在新冠大流行期间对于临床试验所学到的经验教训以及如何利用这些经验构建英国临床试验生态系统并最终使患者获益。
在大流行开始时,MHRA 指派了专门的新冠审评员,并制定了预评估试验文件的流程,因此在方案和支持文件最终...
|
|
BioNTech 推出可全球生产 mRNA 疫苗的廉价可运输模...
2022.02.17
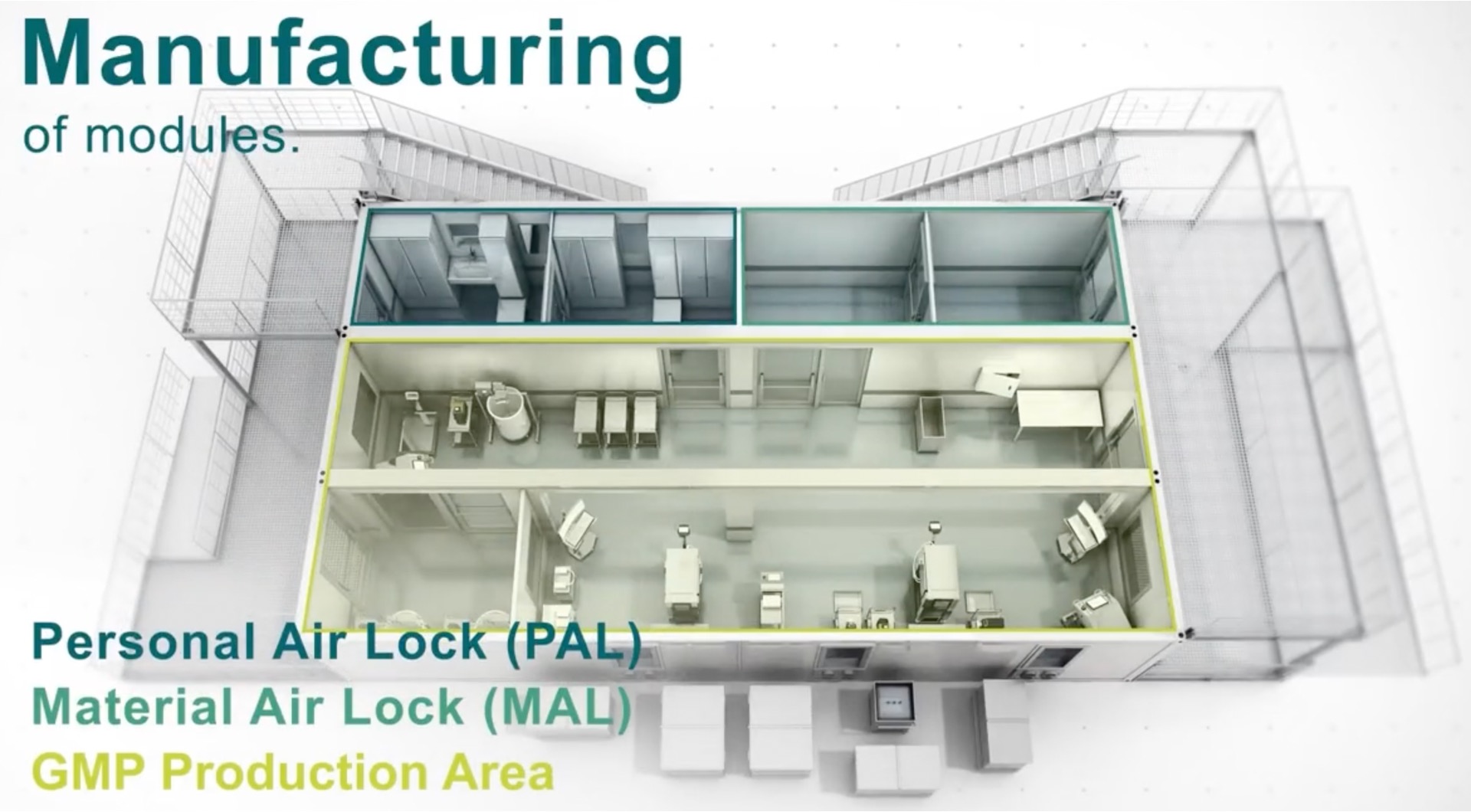
德国 BioNTech 公司于 2022 年 2 月 16 日在一次会议上公布了其在塞内加尔、卢旺达和“可能在南非”的首个“模块化”mRNA 生产设施。
塞内加尔和卢旺达将于 2022 年年中开始建造第一批设施。这些设施是由堆叠的集装箱制成的即用型场地,公司将其命名为“BioNTainer”。该设...
|

|
Robert Califf艰难获FDA局长提名确认,Woodcock将出...
2022.02.16
2022 年 2 月 15 日,美国参议院以 50 比 46 票的微弱优势,正式确认 Robert Califf 为美国 FDA 局长。
这一投票终于结束了 FDA 历史上最旷日持久且最具争议的确认程序。FDA 局长候选人从未有人以如此接近的票差勉强通过确认程序。不过 FDA 总算结束了近 400 天没...
|
|
【识林会议日历】20220215-0228 预告
2022.02.15
识林会议日历
会议是医药产业学习的关键途径之一。会议数量太多,质量参差不齐,没有实时更新提醒的平台,经常会错过一个好会、或在一个不好的会耽误时间,并无处吐槽。
识林会议日历,专门搜集国内外有专业声誉和影响力的会议日程,梳理详细信息和原始链接,并提供评分和评价功能...
|

|
国际药政每周概要:2022.02.07-02.13
2022.02.15
02.11 【FDA】冠状病毒(COVID-19)更新:FDA 推迟咨询委员会会议讨论批准 Pfizer-BioNTech COVID-19 疫苗用于 6 个月至 4 岁儿童
美国 FDA 于 2022 年 2 月 11 日下午表示,取消原定于下周召开的讨论辉瑞幼儿新冠疫苗的专家委员会,以“给 FDA 时间考虑更多数据。”
...
|

|
FDA 公开劝阻企业开发或申请新冠相关“消毒通道”
2022.02.14
美国 FDA 于 2022 年 2 月 8 日发布题为《关于新冠(COVID-19)相关消毒通道的新冠公共卫生紧急政策》指南,公开劝阻申办人开发消毒通道或寻求消毒通道的批准或授权。消毒通道(或消毒隧道、卫生通道)是使用传感器喷嘴向人(及其衣物)喷洒消毒剂或雾化抗菌剂喷雾的通道、走廊、...
|

|
国内药政每周导读:2022.02.07-02.13
2022.02.14
【新药批准和报产】
2.7-2.13,NMPA应急批准辉瑞口服新冠药,CDE受理3个新药上市
【生物类似药】
2.11,CDE发布《生物类似药临床药理学研究技术指导原则》
【市场准入:医保与集采】
2.11,医保局等多部门在国务院政策例行吹风会上谈集采改革进展
【仿制药】
2.1...
|

|
【周末杂谈】信达 PD1 审批与 FDA 的监管套路
2022.02.13
看FDA是如何显示其基于科学、透明公开、合乎法理和长期一致做法的
2月10日FDA的“信达”PD1审批专家会,引起了业内很大的反响。像很多事情一样,开会只是择机向公众发声,思想统一和结论商定是会前的事,即功夫是下在会前的。当然,会上的表现也重要,因为FDA不仅要做正确的事,还要让...
|
|
FDA 宣布推迟下周针对辉瑞幼儿新冠疫苗的专家会
2022.02.12
美国 FDA 于 2022 年 2 月 11 日下午表示,取消原定于下周召开的讨论辉瑞幼儿新冠疫苗的专家委员会,以“给 FDA 时间考虑更多数据。”
FDA 生物制品审评与研究中心(CBER)主任 Peter Marks 和 FDA 代理局长 Janet Woodcock 在一份声明中表示,“基于 FDA 的初步...
|

|
FDA 审批信达 PD-1 药的专委会简报
2022.02.11
编者按: 此肿瘤专家会及近期发生的一些事,显示我国药业的国际化已进入了新发展阶段。如何调整战略战术,无论是对企业还是政府,可能都要从长计议。知己知彼,说起来容易做起来难。关于这个专家会,后续会有各种各样的报道和分析。“识林”希望与大家一道,本着知己知彼的想法,客观、...
|
|
FDA 发布抗体偶联药物临床药理学指南草案
2022.02.10
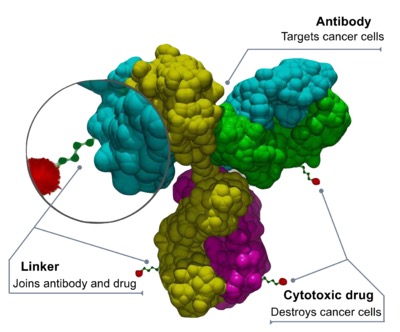
美国 FDA 于 2022 年 2 月 7 日发布了《抗体偶联药物的临床药理学考量》指南草案,向行业和其他参与开发具有细胞毒性小分子药物或有效载荷的抗体偶联药物(ADC)的相关方提供建议。
指南阐述了 FDA 对 ADC 开发计划的临床药理学考虑和建议的当前思考,包括生物分析方法、给...
|

|
欧盟提供控制药物中多种亚硝胺杂质的更多说明
2022.02.09
欧洲药品管理局(EMA)于 2022 年 2 月 4 日发布了修订的问答指南,介绍了上市许可持有人(MAH)应如何识别和控制在药品和原料药(API)中的亚硝胺风险。
指南包含了对之前 2021 年 10 月指南版本的小幅修订。修订后的指南包括应检测的新亚硝胺:N-亚硝胺二丙胺(NDPA),每日...
|

|
美国政府报告建议 FDA 加快招聘海外检查员和翻译服...
2022.02.09
上周,识林资讯报道了美国对海外药企的现场监督检查采取对本土药厂一样政策的立法提案,并讨论了 FDA 国外突击检查试点执行方面的一些预测。本周,美国政府问责办公室(GAO)继续为 FDA 国外突击检查添柴加火,为 FDA 改善国外检查计划提供具体实施建议。
GAO 在 2022 年 2 ...
|

|
FDA 要对中国药企关门了?
2022.02.09
这篇报道里引述的话,不是来自政客(至少不是传统意义上的政客),而是来自科学监管核心部门的核心人,而且说的这么直白,也许对那些在新形势下还想走老路的人会有些触动。
美国 FDA 已安排将在本周四召开专家咨询会议,独立癌症专家将在会上审查 sintilimab 数据。但 Pazdur 已经...
|
|
FDA 发布指南试图缓解毒性研究猴子短缺问题
2022.02.08
美国 FDA 于 2 月 4 日发布了一篇题为《缓解因 COVID-19 大流行引起的非人类灵长类动物供应限制的非临床注意事项》的新指南,帮助研究人员应对与新冠疫情相关的用于进行非临床毒性研究的猴子供应短缺挑战。
目前有数百种针对新冠及相关疾病的药物和疫苗在研,每一个都必须在人...
|
|
FDA 发布群体药代动力学定稿指南
2022.02.07
美国 FDA 于 2022 年 2 月 3 日发布《群体药代动力学》定稿指南,解决了作为新药申请(NDA)、生物许可申请(BLA)或简化新药申请(ANDA)的一部分提交的群体药代动力学(PK)分析的数据和模型要求,另外还涉及 PK 报告的内容和此类分析的标签建议。
2019 年,FDA 修订了已有...
|