
|
药品国际危机事件的防范与应对
2018.09.29
2018年9月2日,第13期识林研习会在北京大学中关新园如期举办,三位资深专家 — James Johnson博士,Garth Boehm博士和尹放东博士,与30余位药企高管和药监人员,从法律、商务和技术角度共议中国药企进入全球市场可能面临危机的预防、应对和控制。【国际危机事件管理的法律、商务和技术考...
|

|
FDA 今年签发更多完全回应函
2018.09.27
2018 财年美国 FDA 对简化新药申请(ANDA)签发了远超过以往任何年份的完全回应函(CRL)。2018 财年到目前为止签发 2515 封 CRL,2017 财年为 1603 封,2016 财年为 1725 封。RAPS 的撰稿人 Zachary Brennan 表示,这可能是由于申请数量激增或其它原因造成的。
但前...
|
|
FDA 知识辅助评估和结构化申请计划提上议程
2018.09.26
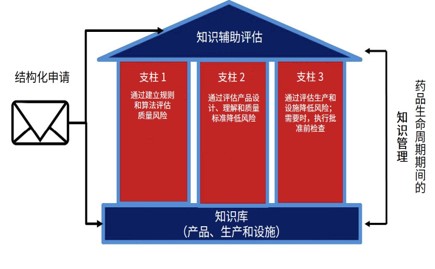
美国 FDA 于 9 月 20 日召开药品科学和临床药理学咨询委员会会议,讨论 FDA 知识辅助评估和结构化申请(KASA)的实施计划。
如 FDA 局长 Scott Gottlieb 在六月份博客中说的那样,KASA 平台旨在将仿制药审评从基于文本的评估现代化为基于数据的评估。但周四的讨论清楚的表明...
|

|
FDA 发布两份指南为药品申请的高质量递交提供建议
2018.09.25
美国 FDA 于 9 月 24 日发布了《ANDA 递交 — 内容和格式》定稿指南。这份长达 32 页的指南比 2014 年的指南草案更详细,提供了对文件某些部分和要求的扩展说明。同时还发布了《NDA 和 BLA 良好审评管理原则和实践》指南草案,向工业界和审评工作人员介绍了在新药审评中审...
|

|
FDA 将对未能公开临床试验数据的企业罚款
2018.09.24
作为生物研究合规监测的一部分,美国 FDA 准备对那些未能向 ClinicalTrials.gov 网站提交临床试验数据的企业罚款。
9 月 20 日发布的新指南草案Civil Money Penalties Relating to the ClinicalTrials.gov Data Bank概述了 FDA 强制执行在 ClinicalTrials.gov 网...
|

|
FDA 药品申请实时审评成为现实
2018.09.21
美国 FDA 已经开始使用药品申请的实时审评,一得到试验结果就立即评估临床数据。这意味着 FDA 可以在申请人提交上市申请后立即批准新的适应症。目前,该方法仅在 FDA 肿瘤卓越中心(OCE)通过两个针对已获批抗癌药的补充适应症的试点项目实施。但之后可能会扩展到新药和新生物制剂。...
|
|
药业高管将大幅抬高药价视为“道德要求”
2018.09.19
一名药业高管为他做出的将一种抗生素混合物的价格提高到每瓶两千多美元的决定辩护,认为“以最高价格销售产品是一种道德要求”。
根据 Elsevier 的 Gold Standard 药品数据库,上个月,位于美国密苏里州的一家小型制药公司 Nostrum Laboratories 一瓶呋喃妥因的价格从 474.75 美...
|
|
复杂仿制药尚无简单解决方案
2018.09.17
复杂仿制药开发研讨会于 9 月 12-13 日在美国马里兰举行。FDA 仿制药办公室(OGD)主任 Kathleen Uhl 在发表主题演讲时表示,复杂药品对于治疗许多严重病症至关重要,例如,多发性硬化症、精神分裂症、转移性乳腺癌、骨质疏松症、慢性阻塞性肺病(COPD)以及糖尿病。其中一些药十...
|
|
FDA 发布 42 篇新 BE 指南和 12 篇修订指南
2018.09.14
美国 FDA 于 9 月 13 日发布了一批 54 篇具体产品生物等效性(BE)指南,42 篇新增,12 篇修订,其中18 篇(12 篇新增,6 篇修订)针对的是非生物复杂药品,14 篇目前没有任何仿制竞争产品。指南详细说明了对于希望开发这些产品的仿制药公司的监管期望,为 FDA 认为证明产品...
|
|
复杂仿制药批准需谨慎,欲速则不达
2018.09.12
【编者按】药监局的基本职责是尽力确保药品标签上的安全和有效性陈述名符其实、让公众感到药品是安全有效的,快审快批其实不是,低价更不是。药监局的公信力离不开自身的职业操守,也离不开全社会的理解、鼓励和支持。
当 EpiPen 的首个仿制药获得批准时,胜利的旗帜在空中飘扬。不...
|

|
FDA 发布原料药批准后变更指南草案
2018.09.11
美国 FDA 于 9 月 10 日发布《原料药批准后变更》指南草案为打算在成品药申请批准后阶段变更原料药生产过程的制药商提供了指导意见。
作为仿制药使用者付费修正案(GDUFA II)重授权的一部分,FDA 承诺发布有关 API DMF(也称为 II 类 DMF)批准后变更的指南,以及引用该 DM...
|

|
为降低药价,医院联合自己造药
2018.09.10
【编者按】为降低医院必备仿制药价格,美国七家大医院联合投资1亿美元成立仿制药生产厂,供自己和其它医院使用。该药厂将是社会公益性的非营利性组织,将保持药价透明,并让药品价格与采购量无关。这个“事极必反”的做法已酝酿多年,总算浮出水面了。效果如何,众人拭目以待。
早在...
|

|
诺华 CAR-T 首次进入英国医保
2018.09.09
英国国家医疗保健体系(NHS)已于 9 月 5 日与诺华就 Kymriah(tisagenlecleucel)达成保险覆盖协议,这标志着欧洲国家首次同意为 CAR-T 疗法提供资金。
诺华在于 8 月 27 日成为首批获得突破性 CAR-T 疗法欧盟上市许可的两家公司之一后不到十天的时间就达成这项协议,成为 NHS ...
|

|
知识-经验-提炼 — IPEM 所学与所用报告会内容简...
2018.09.08
近期“IPEM十年 - 所学与所用专题报告会”上多位IPEM师生将自身所学与项目经验、企业发展相结合,提炼总结,做了精彩多样的报告。识林摘录部分精华如下与大家共飨,报告幻灯片请见此处。本文涉及的主要报告话题有:
GMP 检查在药品质量监管中的运用
国际化市场自营道路的探索
全球...
|

|
英国政府医保体系拒绝覆盖 Gilead 的 CAR-T 疗法
2018.09.06
英国药品成本效益监管机构国家卫生与临床优化研究所(NICE)于 8 月 28 日建议不要在国家医疗保健体系(NHS)内覆盖对 Gilead 公司的 CAR-T 基因治疗药物 Yescarta(axicabtagene ciloleucel)的使用。
之前一天 Yescarta 刚刚获得欧盟上市许可,用于治疗成人患者的两种侵...
|

|
FDA 局长谈监管现代化举措
2018.09.05
(译自 FDA Voice “https//blogs.fda.gov/fdavoice/index.php/2018/08/fdas-comprehensive-effort-to-advance-new-innovations-initiatives-to-modernize-for-innovation/ FDA's Comprehensive Effort to Advance New Innovations Initiatives to Modernize for I...
|

|
IPEM 十年专题报告会 — IPEM 所学所用
2018.09.04
8月31日,IPEM所学与所用专题报告会举行,庆祝国际药物管理工程硕士学位项目(IPEM)办学十周年。报告会邀请IPEM学员和教师代表分享从IPEM项目中学以致用的成功经验、体会和心得,覆盖监管、研发、注册、生产、质量,涉及原料药到药-械组合药品、技术实操到制药国际战略决策实现、制药企...
|

|
2018届北京大学国际药物工程管理(IPEM)硕士项目学位...
2018.09.03
2018年9月1日,2018届北京大学国际药物工程管理(International Pharmaceutical Engineering Management,IPEM)硕士项目学位授予仪式在北京大学中关新园举行。仪式由IPEM教学指导委员和教师Garth Boehm博士主持,北京大学药学院党委副书记吕万良教授,国家药品监督管理局副局长徐景...
|

|
不管叫 CFDA 还是 NMPA,不变的都是局
2018.09.02
【编者按】近期,我国药监从机构、人员、名称都经历较大变化,在北京大学药物国际药物工程管理(IPEM)项目 2018 届毕业典礼上,国家药品管理局徐景和副局长提出变革期的新三定:定势、定位、定力,不管药监局的名称怎么变,不变的是“局”,要在更大的格局上思考药品产业和监管。
...
|
|
美国 FDA 拟制定进口政策降低药价
2018.08.30
美国特朗普政府高级官员于 8 月 20 日表示,一个备受争议的 FDA 工作组已经开始讨论如何从其他国家进口药品,以作为降低美国患者价格的一种方法。药品定价高级顾问 Dan Best 在接受记者电话采访时表示,“该工作组已经启动并正在制定其行动计划。随着更多信息的出现,我们将向市...
|