
|
AAPS年会精彩报告 — 注射剂中的颗粒
2019.11.07
2019年10月17-18日在苏州举办的AAPS中国讨论组年会上,汇聚了近200名来自监管部门、企业、高校的从业者参会。会议期间大家相互学习交流,互动频频。识林和大家分享MSD的Xu Wei博士题为《注射剂中颗粒问题的挑战和机会》的报告,更多会议分享,欢迎大家登录App会议日历【2019年AAPS中国讨...
|
|
关于FDA通过上市后药品安全监督实践努力保护患者的声...
2019.11.06
For Immediate Release November 06, 2019
Statement From Director - Center for Drug Evaluation and Research
Janet Woodcock M.D.
Public health and safety is the highest priority at the U.S. Food and Drug Administration. We maintain a robust practice...
|
|
CAR-T 细胞产品生产质量管理的难点
2019.11.06
CAR-T细胞治疗是当前国内药业发展的重要方向之一,目前国内已有近30家企业,未来还会有更多加入。类似的是,CAR-T类细胞治疗还在研发阶段,就已注定面临激烈竞争;不同的是,细胞、质粒等特殊的工艺控制和无菌操作要求,CAR-T类细胞治疗的工艺合规与质量安全更为重要和困难。
2019年1...
|

|
CRO 相关临床数据欺诈正日益受到美国司法部重视
2019.11.05
美国司法部的执法重点日益集中在与临床试验数据欺诈有关的问题上,尤其是在涉及合同研究组织(CRO)的情况下。司法部消费者保护部门负责人 Gustav Eyler 在食品药品法律研究所(FDLI)最近举行的有关医药产品广告和促销的会议上表达了上述担忧,并指出,在调查涉及虚假和误导性营销的潜...
|

|
FDA 谈产量实时监管, 及海外检查等问题
2019.11.04
随着美国药品和原料药的生产向海外转移以削减成本,质量和可靠性问题日益凸显,美国众议院能源与贸易委员会卫生小组委员会于 10 月 30 日召开主题为“保护全球经济中的药品供应链”听证会,就药品供应链问题聆讯来自 FDA 和其他相关部门的领导者。FDA 药品审评与研究中心(CDER)主任 Ja...
|

|
【更新提示】识林一周回顾(20191027-1102)
2019.11.03
【EMA】新增 亚硝胺杂质概述(10.29) 中译
【EDQM】发给与亚硝胺有关的合成 API 的 CEP 持有人的通知(10.29) 中译
EMA 已要求上市许可持有人采取预防措施,以降低在制造所有包含化学合成活性物质的药物过程中亚硝胺形成或存在的风险。对亚硝胺杂质的评估,分为三个步骤。第...
|
|
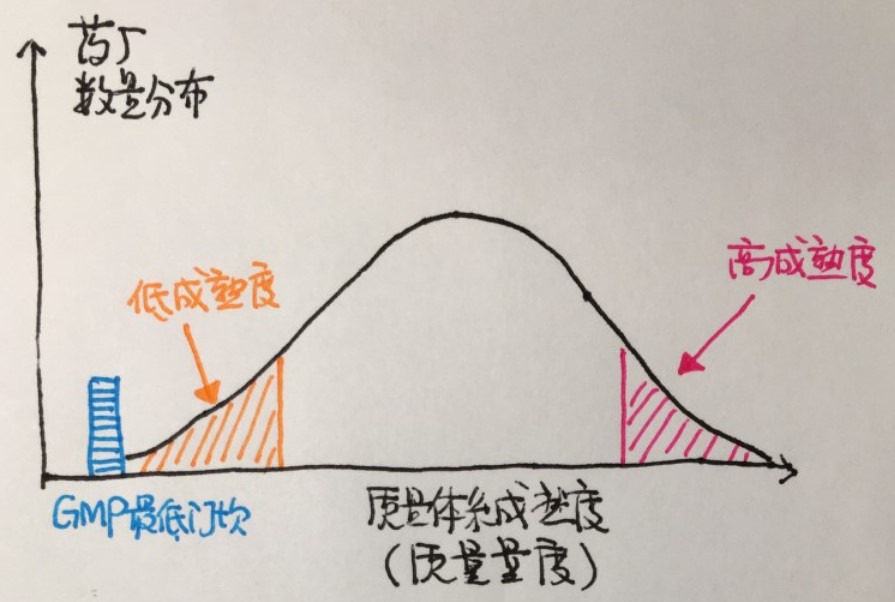
【周末杂谈】FDA再谈“优质优价”
2019.11.03
众所周知,FDA 的使命是保护和促进公众健康,方法是确保产品的安全、有效和质量可靠。但也许不那么众所周知的是,FDA 完成使命的手段是干预跨洲商贸,也就是说采用的是商业手段1,通过建立、维护并改善合理的市场秩序,来促使企业研制和生产有助于公众健康的产品。本文的讨论只限于仿...
|

|
FDA 希望通过数字健康工作组解决药品软件组合产品相...
2019.11.02
随着软件和药之间的联系日益紧密,美国 FDA 已调集其专家人员成立数字健康工作组,以做出政策决定并帮助申请审评人员。该工作组将解决与药品共同使用的软件有关的政策问题。工作组包括来自器械与放射健康中心(CDRH)和药品审评与研究中心(CDER)以及组合产品办公室的代表。
CDER ...
|
|
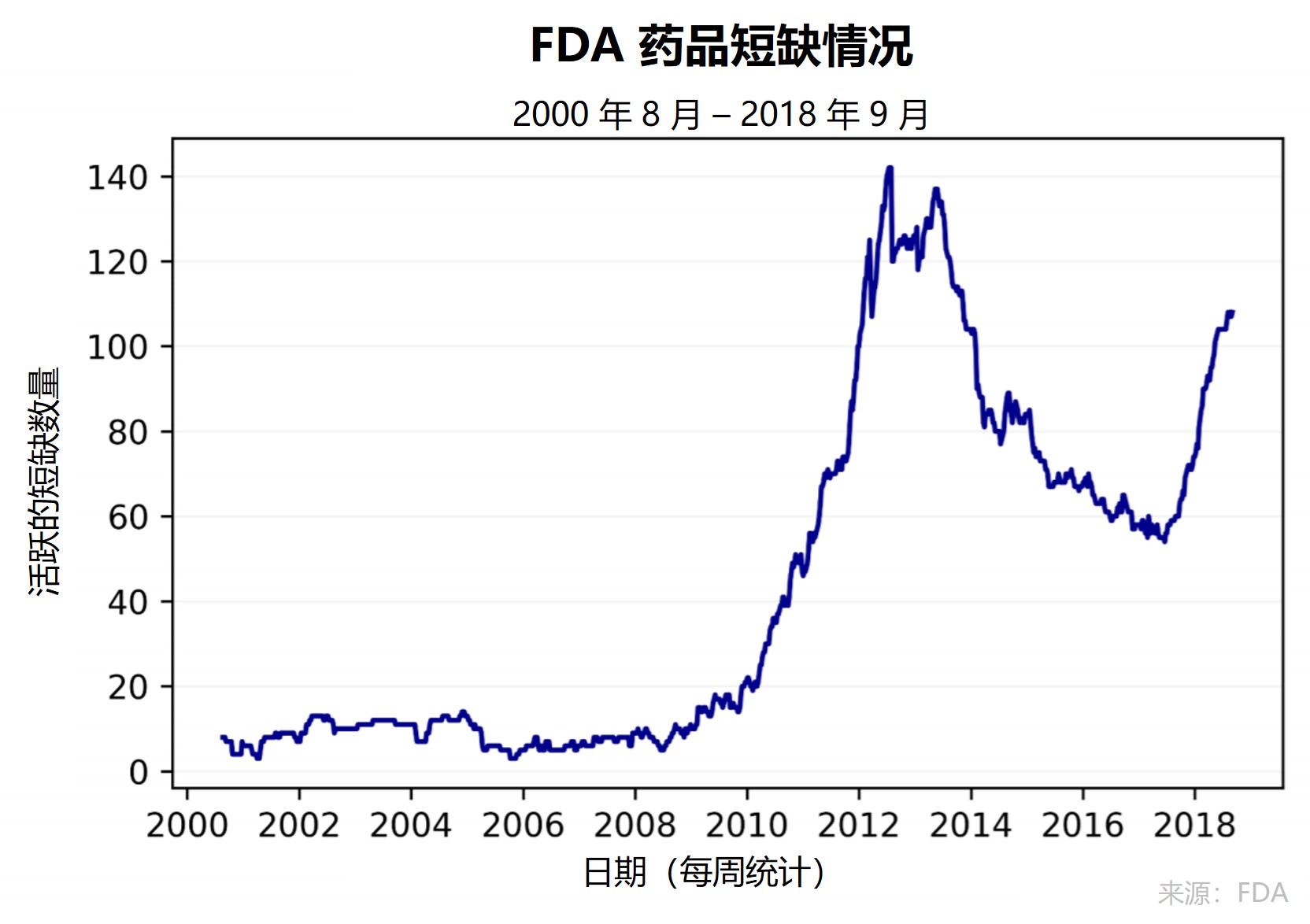
FDA 发布药品短缺根本原因与解决方案报告,能否真正...
2019.11.01
美国 FDA 于 10 月 29 日发布《药品短缺:根本原因和潜在解决方案》报告,讨论了解决药品短缺问题的最新思路。FDA 药品中心主任曾于上周专门撰文预告该报告的发布。【FDA 提出应奖励具有成熟质量体系的制药商以预防药品短缺 2019/10/26】
报告由 FDA 领导的跨机构药品短缺工作...
|

|
FDA 因生物等效性数据问题撤销两 ANDA
2019.10.31
美国 FDA 于 10 月 28 日在《联邦公报》上发布了两份关于撤销简化新药申请(ANDA)批准的通告,原因是 FDA 对申请中所含生物等效性数据缺乏信心。FDA 表示,撤销拟议的依据是,“ANDA 持有人一再未能提交所需的数据来支持对 ANDA 生物等效性的发现。
撤销涉及生物等效性测试实...
|

|
FDA 允许某些组合产品软件通过 DMF 提交
2019.10.30
美国 FDA 于 10 月 28 日发布《CDER 主导的使用电子或软件的器械组成部分的组合产品的 V 类 DMF》指南草案,允许将某些电子或软件组成部分作为药物主文件(DMF)提交来进一步简化组合产品批准流程。
当 FDA 药品审评与研究中心(CDER)主导申请评价时,申报人可以使用 V 类...
|

|
EDQM 发给与亚硝胺有关的合成API的CEP持有人的通知 2...
2019.10.30
Since July 2018, EDQM has been actively involved in activities related to the detection and control of nitrosamine impurities in sartan active substances (APIs) with a tetrazole ring for which there are CEPs. These activities have included contacting...
|

|
德国默克测试机器学习实时平台以预防药品短缺
2019.10.29
最近我们先后聊了美国 FDA 和欧盟对于解决药品短缺问题的最新思路和指南要求,同时,制药商也正在寻找新颖的方法来准确预测需求和控制成本,以预防药品短缺。德国默克正在使用机器学习开展这方面的试验,公司计划与 TraceLink 共同启动一个试点项目,利用公司供应链中的实时数据点来更...
|

|
欧盟关于发现、管理和沟通药品短缺问题的指南
2019.10.28
上周我们介绍了美国 FDA 提议通过评级体系,让采购方可以了解有关药品生产设施生产质量方面的更多信息,从而可以选择向具有成熟质量管理体系的生产商支付更多费用,来奖励生产商在质量方面的投资,更可靠的供应药品,以预防药品短缺。【FDA 提出应奖励具有成熟质量体系的制药商以预防药...
|
|
【周末杂谈】知识工具的作用
2019.10.27
要想了解一个英文词的准确含义,只要打开手机便可上网查询,随时随地。但20年前,在智能手机出现之前,就没那么方便了。那时,我喜欢用Merriam-Webster英文词典,有两本,办公室和家里各一本。办公室里还好办,因为总是伏案工作,桌子上的词典顺手可查。家里就不同了。词典通常放在书房里...
|

|
【更新提示】识林一周回顾(20191020-1026)
2019.10.27
【FDA】指南草案 上市后研究和临床试验—FD&C Act 第505(o)(3)部分的实施(10.25)资讯
指南阐述了 FDA 根据 FD&C 法案第 505(o)(3) 节要求进行某些上市后研究和临床试验(即,上市后要求(PMR))的法定权力,并提供了关于此类研究和临床试验的类型和目的的概述。指...
|
|
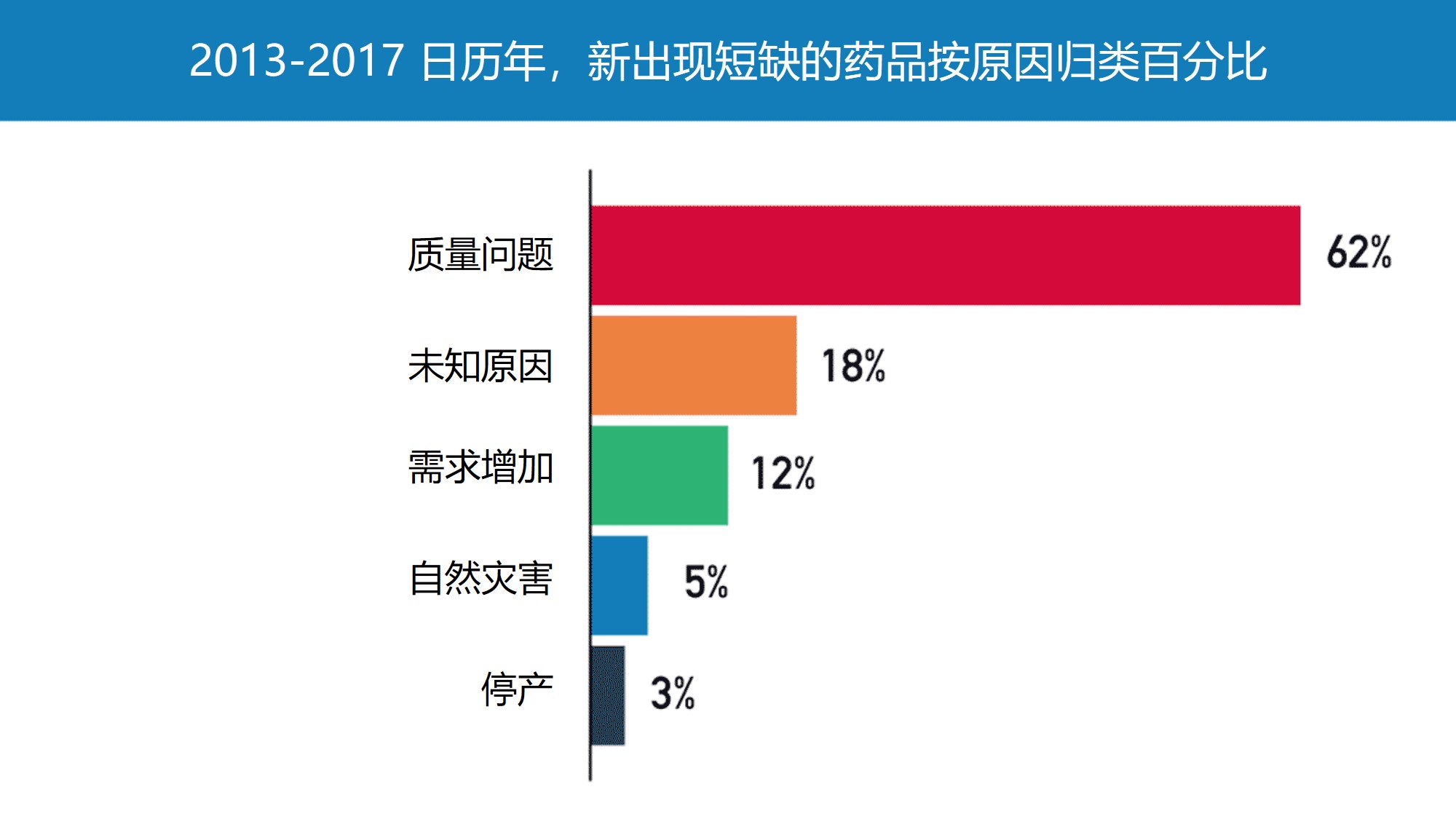
FDA 提出应奖励具有成熟质量体系的制药商以预防药品...
2019.10.26
美国 FDA 药品审评与研究中心主任 Janet Woodcock 于 10 月 24 日撰文表达了通过评级体系,采购方可以向具有成熟质量管理体系的生产商支付更多费用,以预防药品短缺的解决思路。她表示,消费者可能并不总是只根据最低价格购买商品。例如,如果消费者高度重视自己的时间,那么可能...
|

|
FDA 发布关于上市后研究和临床试验要求的指南草案
2019.10.25
美国 FDA 于 10 月 24 日发布题为《上市后研究和临床试验 — 联邦食品、药品和化妆品法案 505(o)(3) 的实施》修订指南草案。如果企业的任何产品有批准后研究要求,则应密切关注该指南文件。
FDA 在介绍指南时表示,“该指南阐述了 FDA 根据 FD&C 法案第 505(o)(...
|

|
FDA 发布有关生产场地信息提交的定稿问答指南
2019.10.24
美国 FDA 于 10 月 22 日发布《在申请中提交给 CBER 和 CDER 的生产场地认定的问答》定稿指南,提供了对由于生产、检测、包装等不完整而引起的一些最常见和最容易出问题的方面的解答。FDA 解释指出,该指南旨在帮助公司了解如何避免提交多余信息、填写到错误位置的信息以及丢失...
|

|
EMA 指明亚硝胺污染的潜在来源
2019.10.23
欧洲药品管理局(EMA)于 10 月 18 日更新“对上市许可持有人(MAH)关于亚硝胺信息”的问答指南,增加第 12 个问题,列出了药品中亚硝胺污染的潜在来源,以帮助企业遵守 EMA 最近对于企业在亚硝胺污染方面的审查和评估要求。
在上月初美国一家在线药房发现赛诺菲的抗酸药 Zant...
|