
|
FDA公布第二次防晒霜吸收的研究结果
2020.01.21
FDA announces results from second sunscreen absorption study
The following quote is attributed to Janet Woodcock, M.D., director of the FDA’s Center for Drug Evaluation and Research.
“Given the recognized public health benefits of sunscreen use,...
|

|
FDA 受新药办公室改组影响的申请
2020.01.21
Applications Affected by the Reorganization of the Office of New Drugs
+
Applications
OND Reorg affected applications p3 (XLS - 2MB)
The approved restructuring of the Office of New Drugs (OND) creates offices that align interrelated disease ...
|

|
敲低髓样抑制细胞GCN2可解除肿瘤微环境中的免疫抑制作...
2020.01.21
肿瘤微环境(Tumor microenvironment, TME)中的癌细胞、T细胞和髓样细胞之间的相互作用是肿瘤发展的关键因素,一般认为,CD8+ T细胞的浸润可抑制肿瘤发展,而髓样抑制细胞(myeloid-derived suppressor cells,MDSCs)和肿瘤相关巨噬细胞(tumor-associated macrophage,TAMs)...
|

|
【更新提示】识林一周回顾(20200113-0120)
2020.01.20
【国家医保局】关于开展第二批国家组织药品集中采购和使用工作的通知(01.17);【政策解读】
国家医保局、国家卫生健康委、国家药监局等部门在总结“4+7”试点和扩围政策、做法基础上,形成了第二批国家组织药品集中采购和使用工作思路。第二批国家组织药品集中采购和使用仍以带量采...
|

|
Keytruda 新增膀胱癌适应症人群
2020.01.20
FDA于2020年1月8日批准PD-1抑制剂Keytruda用于治疗卡介苗(BCG, Bacillus Calmette-Guerin)治疗无效的高风险非肌层浸润性膀胱癌(NMIBC, non-muscle invasive bladder cancer),原位癌(CIS)伴随或不伴随乳头状瘤,且不符合或已选择不进行膀胱切除术的患者。
背景
尿路...
|

|
【周末杂谈】读纽约时报社论:困境中的FDA
2020.01.19
2020年1月11日,美国纽约时报发表社论“困境中的FDA。如何改进 - 对新局长的工作建议”(The FDA Is in Trouble. Here's How to Fix It - Some New Year’s resolutions for the incoming boss),对FDA近年来的一些所作所为,提出了尖锐的批评。请注意,纽约时报...
|

|
FDA 药品中心主任谈在云端建立全球质量档案
2020.01.18
美国 FDA 药品审评与研究中心(CDER)主任 Janet Woodcock 指出,解决日益严重的国际药品制造质量要求冲突问题的唯一途径是建立全球质量档案。
她在 12 月份的 PDA 质量风险管理会议上分享了关于这一愿景的一些想法,如果实现这些想法,不仅可以简化新药的生产,而且可以持续...
|

|
欧盟药品短缺网络试点进入第二阶段
2020.01.17
欧洲药品管理局(EMA)和药品机构(HMA)于2016年12月成立了HMA/EMA人用和兽用授权药品供应https//www.hma.eu/522.html 特别工作组,以提供战略支持和建议,来解决人用药和兽药供应中断的问题,并确保其持续供应。其主要优先事项包括
研究如何利用现有的监管框架(例如,通过工...
|

|
FDA利用技术和合作来支持罕见病药品研发
2020.01.17
FDA Harnesses Technology and Collaboration to Support Rare Disease Product Development
Announcing an Orphan Drug Technology Modernization effort and the 2020 FDA Rare Disease Day meeting
By Amy Abernethy, M.D., Ph.D., Principal Deputy Commissione...
|
|
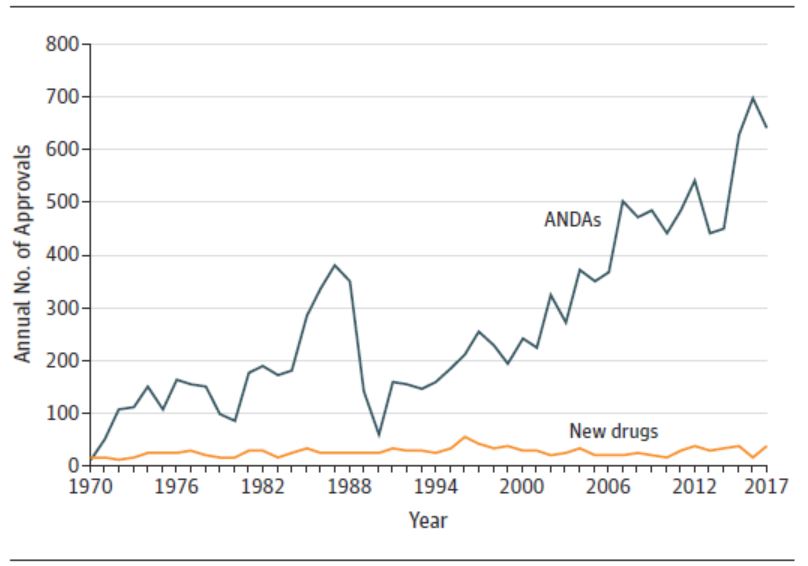
过去四十年 FDA 新药审批改革成效如何,需再次改革...
2020.01.16
1 月 14 日发表在 JAMA 上的一篇题为“1983-2018 FDA 药品批准和监管”的通讯文章引发了业界的广泛关注,文章认为美国 FDA 在过去四十年中进行的加快审评的改革可能需要进一步做出改变。文章作者为哈佛医学院布莱根妇女医院医学系的 Jonathan Darrow 等人。
总体而言,文章...
|

|
“液体活检”技术又有新突破 — ctDNA的甲基化标记...
2020.01.16
结直肠癌(colorectal cancer,CRC)是全世界第三大高发的致命癌症,与所有癌症一样,越早得到确诊和治疗,患者预后越好、生存率越高。通常认为,肠镜检查是CRC早期诊断和筛查的最佳检测方法,但由于其侵入性较强,且有可能导致并发症,往往会使病人产生抗拒心理。因此,尽早发现具备高特...
|

|
FDA 新十年的大麻政策
2020.01.15
Cannabis Policies For the New Decade
Testimony of
Douglas Throckmorton, M.D.
Deputy Director for Regulatory Programs - Center for Drug Evaluation and Research CDER
Before the
https//energycommerce.house.gov/subcommittees/health-116th-congress...
|

|
中国和PICS的2020工作计划
2020.01.15
2020年1月1日,PIC/S迎来了第53个成员机构,意大利兽医药局(Italian Veterinary Agency, DGSAF)。另外巴西已经接近了PIC/S评估程序的尾声,而俄罗斯已经完成了预评估程序。被选任2020-2021年PIC/S主席的Anne Hayes在去年12月30日的发布会上,谈到了2020年PIC/S的计划和优先级。Ha...
|
|
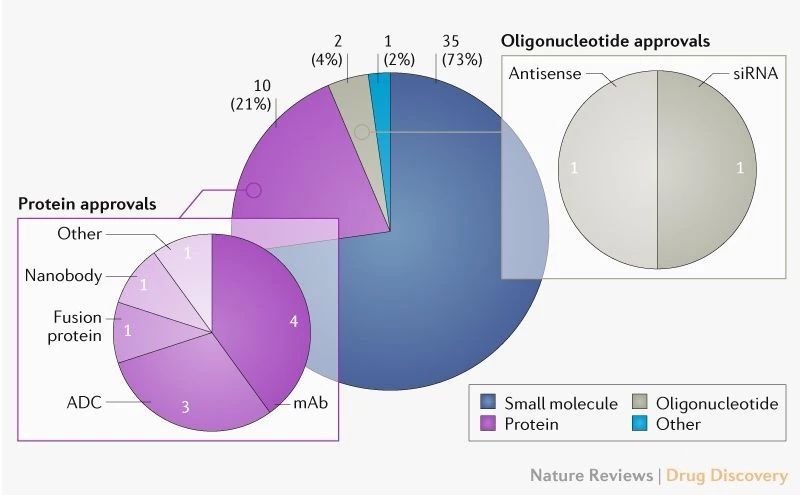
【转载】Nature子刊:2020年FDA可能批准的新药
2020.01.14
2019年,FDA 的药品评价与研究中心(CDER)共批准了48款新药上市,虽然数量上低于2018年的59个,但是这个数字仍是过去25年的第3高。FDA最近连续5年的平均批准新药数量达到了44个,这个数字是2005-2009年平均批准新药数量(22个)的2倍。
FDA在新药审批方面给予的政策激励也能解释...
|

|
2019 年中国企业不合格 483(OAI)细读
2020.01.14
注:在研究过程中,我们发现FDA提供的清单存在显著缺失,不少识林483数据库中已经收录的483并没有在其中体现,FDA对此备注说:并非所有的检查都收录在数据库里,不包括州检查、批准前检查、专论设施检查、等待最终执法行动的检查和非临床实验室检查。如果大家还发现有其它类型的缺失信息,...
|

|
【更新提示】识林一周回顾(20200106-0112)
2020.01.13
【NMPA】国家药监局综合司公开征求《化学药物中亚硝胺类杂质研究技术指导原则(征求意见稿)》意见(01.11)
指导原则指出申请人应切实履行药品质量管理的主体责任,对药品的安全和质量进行全生命周期管理,尽可能的避免亚硝胺类杂质的引入,若确不能完全避免的,应充分评估药品中亚硝...
|
|
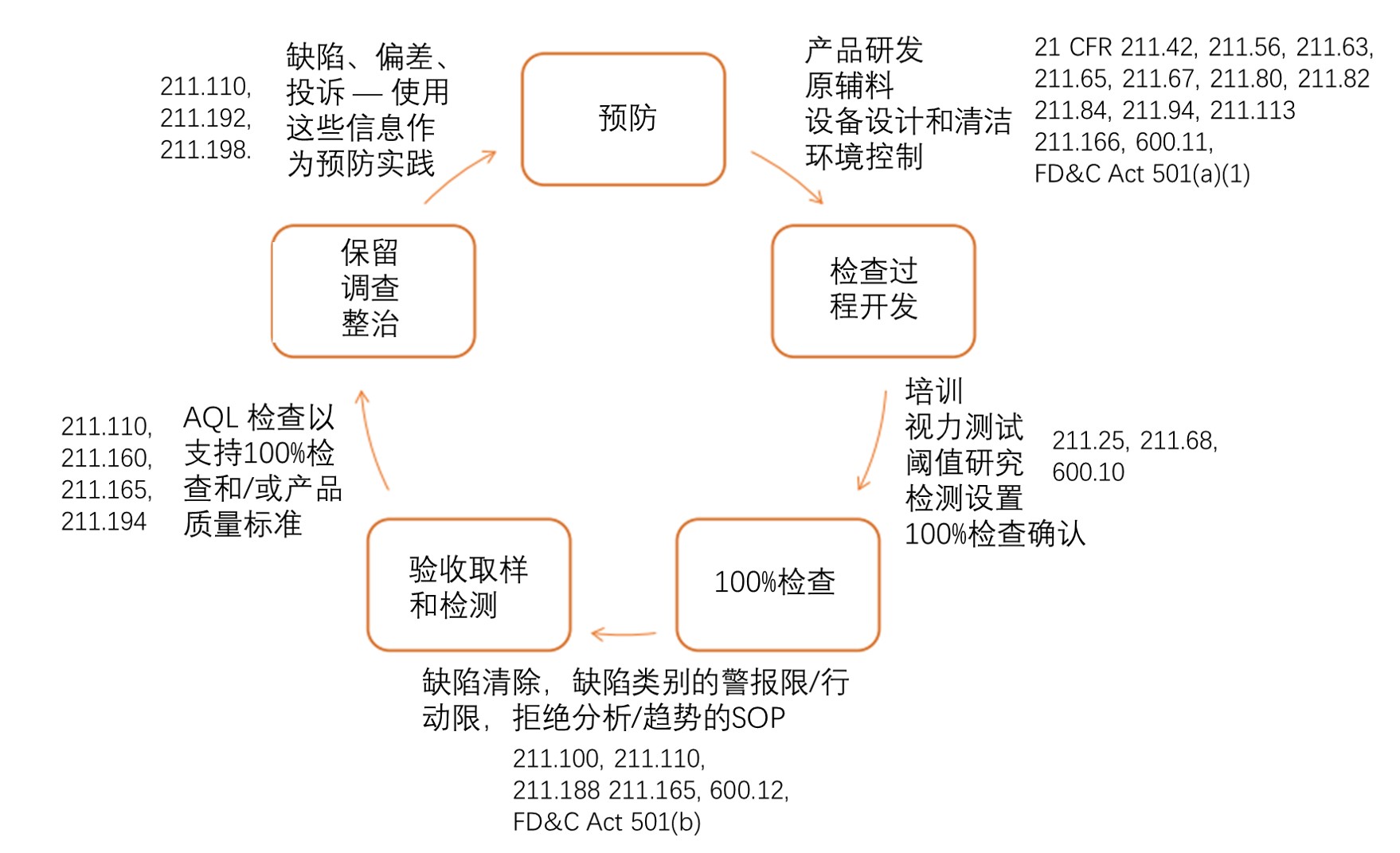
可见颗粒物污染的生命周期解决方案
2020.01.13
可见的颗粒物污染是导致注射剂批次被拒绝或召回的主要原因之一,在2009年至2019年间,发生在美国的注射剂召回事件中,存在异物颗粒问题是仅次于缺乏无菌性保证的原因。美国注射剂协会(Parenteral Drug Association, PDA)2015年对注射剂生产商的调查显示,上年度:
43%的受访者由...
|

|
【周末杂谈】OAI、透明公开监管与产业发展
2020.01.12
上月11日,在美国食品药品法研究所在华盛顿举行的一次会议上,FDA药品审评和研究中心合规办公室(Office of Compliance,OC)主任D. Ashley高兴地报告,2019财年(9月30日截至),在GMP检查后90天(本文引用的都是自然天,不是工作日)内,OC完成了86%的检查结果分类,比2018财年增加...
|

|
【全文翻译】2019 年 FDA 新药审批总结报告
2020.01.11
美国 FDA 于 2020年 1 月 6 日发布了 2019 年度新药审批总结报告,报告汇总了 FDA 药品审评与研究中心(CDER)去年批准的所有新药、新用途和新适用人群,以及生物类似药、新配方和新剂型药物,概述了一系列值得注意的批准,提供了许多 CDER 批准的新治疗药物促进患者健康的有...
|

|
创新药 MAH 早期临床阶段需要什么程度的质量体系?
2020.01.10
MAH推进和创新药热潮,催生生产和检验完全外包的虚体药企。那么问题来了,这些企业在早期临床,具体来说就是临床I期,需要什么程度的质量体系呢?具体而言,需要多少个SOP呢?尤其是全生命周期GMP管理理念的盛行,可能产生两极分化,造成资源浪费和效率低下,甚至本末倒置 – 临床I期的...
|