
|
FDA 表示生物类似药生产场地更需要现场检查而不是远...
2022.11.15
美国 FDA 药品审评与研究中心(CDER)首席副主任 Jacqueline Corrigan-Curay 在前不久普享药协会(AAM)举行的 GRx+Biosims 会议上表示,对于生产生物类似药的工厂,将会执行现场检查而不是远程评估,因为这些产品相对较新,并且涉及到新颖的生产工艺。另外,会上还讨论了生物类...
|

|
国内药政每周导读:新药获益-风险评估,药品注册期间...
2022.11.14
【创新药与临床研究】
11.08,【CDE】关于公开征求《儿童抗肿瘤药物临床研发技术指导原则》意见的通知
11.08,【CDE】关于公开征求《新药获益-风险评估技术指导原则》意见的通知
【药学研究与仿制药】
11.08,【CDE】关于发布《化学仿制药口服调释制剂乙醇剂量倾泻试验...
|

|
FDA 2022 财年仿制药批准数据趋势与分析
2022.11.14
美国 FDA 仿制药办公室(OGD)最近更新了 2022 财年全部仿制药使用者付费(GDUFA)批准和接收数据。2022 财年 FDA 共完成 722 件简化新药申请(ANDA)完全批准,比去年多出 43 件,但也不及前几年,比 2019 财年创造了历史最高批准记录的 935 件更是少了 213 件。原始 ANDA...
|

|
【周末杂谈】咬文嚼字:临床试验与临床研究
2022.11.13
公开临床试验数据,借助社会资源,了解药品的真实疗效
ICH E6(R2) GCP指导原则说:“The terms clinical trial and clinical study are synonymous”,即临床试验和临床研究是同义词。笔者以为这个说法是狭义在GCP范畴内的,反映了ICH本身的注册偏向性,及产业界的利益所在...
|

|
【识林主题词】新建:远程检查,FAT-SAT;修订:召回...
2022.11.12
— 主题词源于对大量法规、文献、案例、问答的综合分析,并从概述、法规指南、实施指导、视频、问答、案例、参考资料等多维度呈现。
— 区别于散点化的法规和技术资料,主题词是精炼沉淀的知识汇编,旨在帮助识林企业用户开展系统学习,将外部知识有效地转化为内部认知,切实提升业...
|
|
亚硝胺潘多拉魔盒已经打开,仿制药行业呼吁 FDA 以...
2022.11.11
自 2018 年在降压药缬沙坦中发现亚硝胺杂质以来,问题不断升级,影响的产品范围不断扩大,包括一系列沙坦类药物,胃灼热药雷尼替丁和尼扎替丁,2 型糖尿病药物二甲双胍和西格列汀,结核药利福平和利福喷丁,戒烟药 Chantix……所涉药品既有仿制药也有品牌药。这让全球监管机构和行业都...
|

|
百时美施贵宝重磅抗癌药Abraxane生产厂因反复培养基灌...
2022.11.11
美国 FDA 在 10 月 30 日签发给 Abraxis Bioscience 公司的信中列出了与该公司价值数十亿美元的重磅抗癌药 Abraxane(白蛋白结合型紫杉醇)相关的一系列生产问题。
Abraxis Bioscience 于 2010 年被新基(Celgene)收购,百时美施贵宝(BMS)通过在 2019 年以 740 亿美元收购...
|
|
FDA 质量管理成熟度计划新进展
2022.11.10
2022年11月2至3日,FDA举办了为期两天的药物科学与临床药理学咨询委员会会议。会议重点讨论了与药品质量办公室(OPQ)促进美国公众获得优质药品的使命相关的两个关键主题:质量管理成熟度(QMM)和KASA。本文将介绍关于QMM的主要讨论内容。
link=13px
-->
11月2日,委员会讨...
|

|
临床试验结果公开:美国立卫生研究院开始对未遵守报告...
2022.11.10
最近几周,美国国立卫生研究院(NIH)开始对未能向政府数据库提交临床试验结果的学术机构发送电子邮件。
临床试验注册和结果报告工作组表示,截至本周,NIH 已联系了二十多家机构。该工作组是一个由学术医疗中心、大学、医院和非营利组织组成的国家联盟,专注于临床试验的透明度。工作...
|

|
FDA 发布仿制药活性成分的相同性评估指南草案
2022.11.09
美国 FDA 于 11 月 8 日发布了业界期待多年的指南草案“ ANDA 中的相同性评估 - 活性成分”,旨在帮助准备简化新药申请(ANDA)的申请人在证明拟议仿制产品中的活性成分与参照上市药品(RLD)之间的相同性方面提供建议。
这篇指南自 2019 年起就一直列在 FDA 计划发布的...
|

|
最高法院拒绝受理 BMS 诉吉利徳的 CAR-T 专利侵...
2022.11.09
昨日我们报道了美国最高法院同意受理安进诉赛诺菲关于高胆固醇治疗药 PCSK9 单抗的专利侵权案,而紧接着最高法院驳回了百时美施贵宝(BMS)子公司 Juno 诉吉利徳的 CAR-T 专利侵权案的审理请求。
先简单说一下这个案子的情况:2017年,Juno(BMS 旗下)对Kite pharma(吉利德...
|
|
美最高法院受理安进和赛诺菲关于高胆固醇治疗药 PCSK...
2022.11.08
美国最高法院最近同意审理安进(Amgen)关于认为联邦巡回法院错误地确定其关于胆固醇药物专利无效案件的上诉。
这是安进与竞争对手赛诺菲(Sanofi)及其合作伙伴再生元(Regeneron)之间在可注射胆固醇治疗市场上长期专利斗争的最新进展。安进于 2014 年起诉赛诺菲,指控赛诺菲前蛋...
|

|
国际药政每周概要:FDA肿瘤药联合用药方案交叉标签指...
2022.11.08
【注册、审评、审批】
11.03【FDA】指南定稿 联合用药方案中的交叉标签肿瘤药
【创新研发与临床】
11.04【FDA】指南定稿 在早期临床试验中研究细胞或基因治疗产品的多种版本
11.01【FDA】指南草案 治疗用临床试验用药物的扩展应用:问答
【GxP 与检查】
【监...
|

|
国内药政每周导读:药品注册电子申报,细胞GMP指南落...
2022.11.07
【药学研究与仿制药】
11.02,【CDE】关于发布《儿童用药口感设计与评价的技术指导原则(试行)》的通告(2022年第37号)
【注册,审评,审批】
10.31,【NMPA】关于国家药监局批准药品电子注册证统一使用“国家药品监督管理局药品注册专用章”电子印章有关事宜的通知
11....
|
|
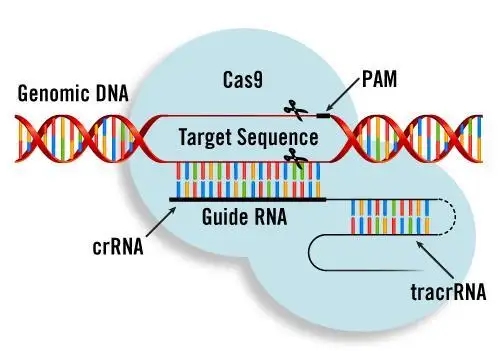
CRISPR 疗法治疗杜氏肌营养不良试验的唯一受试者死亡...
2022.11.07
非营利组织 Cure Rare Disease(CRD)用于治疗杜氏肌营养不良症(DMD)首个人体 CRISPR 疗法在获得 FDA 临床许可的两个月后,该组织宣布试验中唯一的一名患者去世,这名 27 岁的患者 Terry Horgan 也是组织创始人兼首席执行官 Rich Horgan 的弟弟 。
CRD 尽管研究者...
|

|
【周末杂谈】百忧解 - 跌下神坛的药
2022.11.06
好到难以置信的事,也许还是慎信为好
10月7日,美国银行(BoA)分析师称,礼来公司治疗糖尿病和减肥新药Mounjaro(通用名Tirzepatide)有望成为世上首个年销售额达 1000 亿美元的药。这是什么概念?据世界银行2020年数据,在全球194个国家中,2/3多的国家GDP低于这个数。
今年5月,...
|

|
【识林翻译】PICS的GMP通则,FDA变更可比性方案,原液...
2022.11.05
识林里,中外法规指南浩如烟海。识林用户的第一步,往往是从本职工作出发,检索、阅读和使用。即使没有出口业务的用户,也可开展系统性学习,遍读各国法规,形成对重要知识点的深度认知。为帮助用户跨越语言关,加深理解,识林翻译团队(也包括向导)将努力为识林企业用户提供法规指南...
|
|
辉瑞呼吸道合胞病毒(RSV)母体疫苗3期试验证明对新生...
2022.11.04
辉瑞于 11 月 1 日表示,针对呼吸道合胞病毒(RSV)的母体疫苗将新生儿重症发病率降低了 81.8%,达到研究目标。辉瑞表示,计划在今年年底前向 FDA 提交有关疫苗的数据,并预计将收到 8 个月的审评目标日期。
RSV 是小婴儿患病和感染的常见原因,且小婴儿感染出现严重疾病...
|

|
FDA 发布联合用药方案中的交叉标签肿瘤药定稿指南
2022.11.04
美国 FDA 于 11 月 2 日发布了《联合用药方案中的交叉标签肿瘤药》定稿指南,对于被批准用于联合用药方案的肿瘤药标签中应包含的信息提供建议。
肿瘤学中的药物批准通常通过在当前治疗方案中添加药物或通过在联合用药方案中组合研究用药来建立治疗效果,从而创造出更有效的新方...
|

|
FDA临床决策支持软件定稿指南解读:进一步退两步,问...
2022.11.03
美国 FDA 于 9 月底发布了一系列于软件、自动化和人工智能相关的指南文件,其中包括一份关于临床决策支持(CDS)软件的定稿指南,10 月 18 日 FDA 举行了一次网络研讨会对该定稿指南提供了更多说明。盛德律所最近发布了对这一指南的解读,下面我们详细来看看。
盛德指出,这...
|