
|
【轻松一刻】带幻觉的 AI 并非真正风险
2026.05.02
*改编自GMP专家Ian Thrussell分享的素材。
AI为什么会有幻觉?
AI不懂,只是一味地猜。
它选最“靠近”的词,不是最靠谱的话。
文字有空,它就填。
数据有缺,它就编。
它没有“不知道”这个选项——
宁可胡说,绝不沉默。
其实,我们也有份
我们...
|

|
美待定法案禁止 IND 采用中国临床数据
2026.05.01
*识林读者和会员五一节日快乐!识林将在假期保持每日一篇更新。
4月29日,美国国会众议院拨款委员会在FDA相关的联邦支出法案报告中添加条款,禁止FDA"接受、审评或考虑"来自中国、俄罗斯、伊朗或朝鲜的临床试验数据。该禁令明确适用于新药临床试验申请(IND)。
委员会在报告中...
|

|
AI 加持下,FDA 试点“实时临床试验”
2026.04.30
4月28日,FDA宣布实施"实时临床试验"(Real-Time Clinical Trials,RTCT)试点,基于其已开展的两个概念验证临床试验,计划于今年夏天启动更大范围的RTCT试点项目。
简言之,FDA设想的RTCT是利用AI和电子健康记录技术的进步,将临床试验中原本需要人工从试验记录中提取、手动录...
|

|
FDA 强令 Tavneos 撤市,严厉指控药企操纵临床数据
2026.04.30
4月27日,FDA在一封信函中严厉指控ChemoCentryx(现为安进Amgen旗下公司)操纵了Tavneos(阿伐可泮)的关键临床试验数据,并要求安进将该药撤出市场。安进再次明确拒绝撤市,使其与监管机构陷入罕见的高风险对峙。
Tavneos用于治疗活动性抗中性粒细胞胞浆抗体(ANCA)相关性血管炎,...
|

|
英国落地临床试验全面改革,聚焦 FIH 启动速度
2026.04.29
4月28日,备受期待的英国临床试验新法规正式生效。其被视为该国二十多年来最重要的临床试验法规全面修订,引入了全新的试验审批和监管方法。
英国药品和健康产品管理局(MHRA)在公告中指出,将加速评估首次人体试验(First in Human,FIH),并引入“可通知试验”(notifiable tri...
|

|
FDA 年报显示药企稳定履行 PMR 和 PMC
2026.04.29
4月24日,FDA发布《2024财年药品和生物制品公司在执行上市后要求和承诺方面的绩效报告》。报告显示药企对于上市后要求和承诺(PMR/PMC)的履行情况整体良好可控。
PMR是根据法规要求必须开展的研究或临床试验,而PMC是申请人自愿承诺且书面同意开展的研究或临床试验。临床试验成本高...
|

|
GMP 环境中用 AI:案例分析与合规范式转变
2026.04.28
近日,路易斯安那大学拉法叶分校的研究者发表文章《制药中的人工智能:应用、案例研究及 GxP 实施考量》,综述了AI在药品制造领域应用的最新进展,包括8个案例分析以及在应对GMP合规挑战方面的洞见,可为我国药企在生产线上合规且高效地应用AI提供参考。
站在药企角度,研究者指出...
|

|
FDA 合规办公室年报:警告信激增至314封,主因并非生...
2026.04.28
4月23日,FDA合规办公室(OC)发布《2025年合规办公室年度报告》(本该去年发布的2024年报被跳过),概述了该办公室在药品生产设施合规监管、临床试验监管、生物研究监测等方面的工作成果。报告显示,FDA在2025年的合规行动显著增加,特别是针对未经批准或错标的药品违规行为以及药品掺...
|

|
国际药政每周概要:FDA 总结动物试验减免,合规办公...
2026.04.28
【非临床与临床研究】
4.20,【FDA】减少非临床研究中的动物试验:首年进展与未来之路
4.20,【SFDA】利用真实世界数据(RWD)和真实世界证据(RWE)支持药品上市许可有效性与安全性的框架
【药学研究】
4.24,【WHO】口服速释制剂的生物等效性(征求意见稿)
本周BE指...
|

|
《药品附条件批准上市申请审评审批工作程序》的要点沿...
2026.04.27
4月24日,NMPA定稿了业界瞩目的《药品附条件批准上市申请审评审批工作程序》(“41号文”),取代了2020年7月发布的原版文件(“82号文”)。文件经历过2023年8月和2025年7月两次征求意见,可谓慎重。
另外特别值得一提的是,两份意见稿以及现行版均附带相应的“政策解读”,对正文内...
|

|
再生元终签 MFN 协议,其基因疗法获61天快速批准
2026.04.27
4月23日,再生元(Regeneron)成为第17家与特朗普政府签署最惠国(Most Favored Nation,MFN)药价协议的大型药企,也是收到特朗普邀请的最后一家。
同日FDA批准其基因治疗药物Otarmeni用于OTOF基因相关听力损失的超罕见病,美国每年约有50名新生儿受此影响。这是全球首个用于听力...
|

|
国内药政每周导读:附条件批准新规落地,重大变更注册...
2026.04.27
【CMC药学研究】
4.20,【NMPA】关于发布仿制药参比制剂目录(第一百零四批)的通告(2026年第12号)
【注册与变更】
4.20,【CDE】关于公开征求 ICH《M8:电子通用技术文档(eCTD)v4.0》指导原则及问答文件中文翻译稿意见的通知
4.20,【CDE】关于发布《治疗用重组蛋...
|

|
【周末杂谈】美国是靠不住了,靠中国吧,又怕哪天被甩...
2026.04.26
从ISPE欧洲年会,看欧洲对美国的失信、中国的崛起、及自身发展的看法
近来,美国和英国方面不时发声中国药业的崛起(参考识林报道1、2、3)。考虑这两国间的密切关系、及与我国的敏感竞争和合作关系,对这些声音有时不得不从多角度理解。相比之下,欧洲小些的、较为中立国家的声音,可能...
|

|
【直播】26年4月全球法规月报划重点
2026.04.25
识林2026年4月报直播如期而至,并同步推出4月报。本次直播聚焦4月全球主要监管机构的重点法规,并挑选影响力较大的文件做重点简介。短短40分钟,轻量而轻松,旨在帮助大家回顾上个月的监管重点,加深理解或是查缺补漏。
月报获取渠道:
会员:关注直播当日(5月8日,周五)的【最近更...
|

|
【课程与会议】近期更新的重点课程和5-6月会议预告
2026.04.25
近期更新重点课程
识林升级版用户,可在PC端和App、小程序移动端学习57个模块的1000+门课程7000+节视频,涉及药品研发、注册、生产、质量等全生命周期,包括IPEM项目部分精华课程摘要,监管和学术机构专题教学和研讨会,及供应商技术介绍专业课程。除视频内搜索、收藏、评论功能外,...
|
|
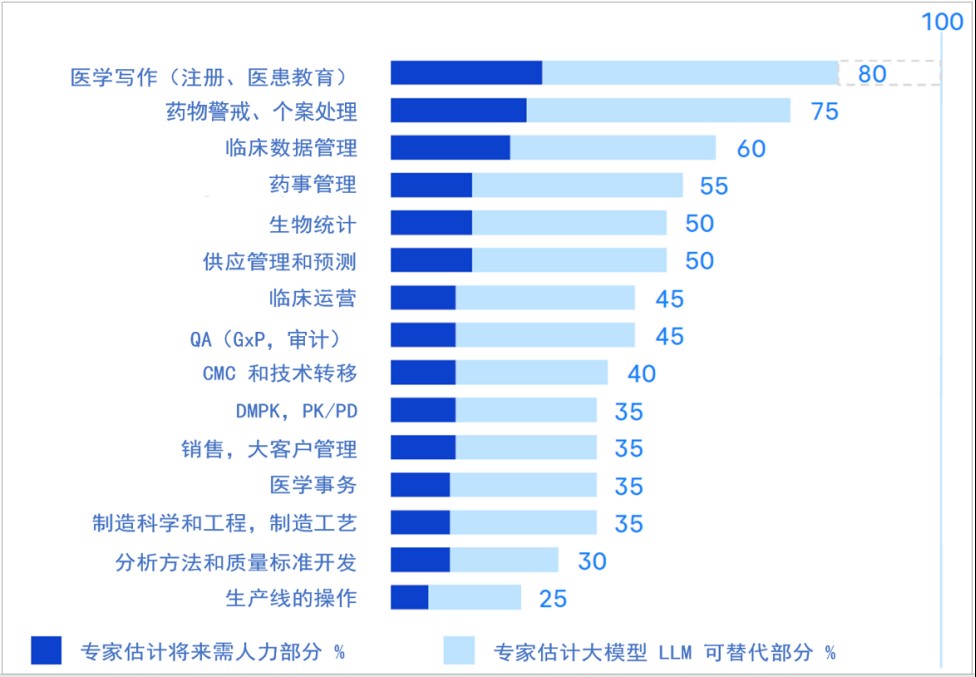
AI – ISPE 欧洲年会上无所不在的话题
2026.04.24
今年的国际制药工程协会(ISPE)欧洲年会于本周一至三在丹麦哥本哈根市举行。AI是会议热点之一。报告题目中含AI字眼的专题分会场多是座无虚席,边上和后面都站着人。题目中不含AI字眼的主会场报告也有不少与AI相关。由于主会场的报告人往往是业内资深人士,责任和影响都大,他们对AI的看法值...
|

|
FDA 公开完全回应函做法首次引来药企发难
2026.04.24
在法律边界模糊不清的背景下,制药行业首次针对FDA公开完全回应函(CRL)政策发起挑战。4月20日,Covington & Burling律师事务所代表一家匿名制药公司提交了公民请愿书,要求FDA建立一个正当程序框架,在FDA披露针对待审批或撤回的新药申请(NDA)、简化新药申请(ANDA)和生物制品许...
|

|
FDA 总结动物试验减免和 NAM 应用,规划后续8个行...
2026.04.23
4月20日,FDA发布《减少非临床研究中的动物试验:首年进展与未来之路》(Reducing Animal Testing in Nonclinical Studies Year One Progress and the Path Forward)报告。该报告系统梳理了FDA自2025年4月发布《减少临床前安全性研究中动物试验的路线图》(Roadmap to Reducing Ani...
|

|
沙特 FDA 的 RAID:面向“全球新”药物的优先审评...
2026.04.23
4月5日,沙特食品药品管理局(Saudi Food and Drug Authority,SFDA)发布了《研究与试验用药物(RAID)认定》指南。RAID计划旨在加速未获任何其他监管机构上市许可的创新药(“全球新”)的开发与审评。该指南将于2026年7月2日正式生效,自此SFDA加入了主流药监追求全球新药的行列。
...
|

|
发酵或半合成抗生素杂质:FDA 要求做毒理,中欧设具...
2026.04.22
4月17日,FDA发布题为《建立抗生素的杂质质量标准》(Establishing Impurity Specifications for Antibiotics)的指南草案。
FDA指出,完全通过化学合成生产的抗生素应遵循ICH Q3A、Q3B及M7指南中关于杂质和降解产物的控制原则(识林会员可登录ICH索引页面查阅本文提及的ICH指南...
|