
|
FDA 竞争性仿制药指南定稿版本与草案有哪些不同?
2020.03.17
美国 FDA 于 3 月 13 日发布《竞争性仿制药》定稿指南,介绍了 FDA 竞争性仿制药(CGT)认定的内容、何时适用以及如何应用等关键要素。CGT 认定是根据 2017 年《FDA 重新授权法案》(FDARA)建立的,旨在激励缺乏竞争的仿制药的开发。FDA 局长 Stephen Hahn 表示,“CGT ...
|
|
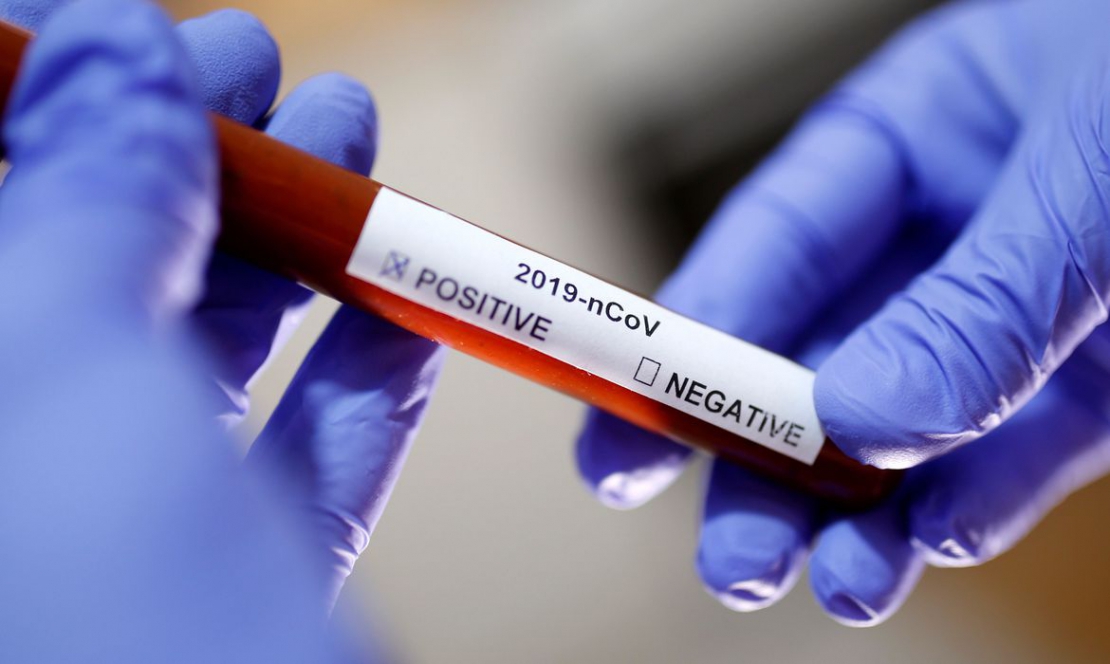
从 USP 标准品订单一窥疫情下中印药品生产现状
2020.03.16
美国药典(USP)首席执行官 Ron Piervincenzi 日前表示,中国的药品生产地区从 2 月中旬已经开始从与新型冠状病毒肺炎(COVID-19)疫情有关的旅行限制中恢复,产量已经恢复到正常水平的一半。USP 可以通过检查其参照标准品在中国境内的销售情况来窥探到生产恢复的情况。
他表示...
|

|
【更新提示】识林一周回顾(20200309-0315)
2020.03.16
上周随着 WHO 宣布新型冠状病毒肺炎(COVID-19)疫情全球大流行,各药监机构纷纷出台各种应对措施和指南,本文中开辟新板块“新冠疫情全球监管应对”集中回顾。国家局发布 MAH 和生产企业追溯基本数据集等 5 项信息化标准。FDA 发布评估 2 型糖尿病治疗药安全性的新指南,不再...
|

|
【周末杂谈】一位美国专业人士在抗击COVID-19疫情中...
2020.03.15
迫于疫情恶化和各方重压,美国政府周五宣布进入国家紧急状态。继美联储3月4日降息半个百分点(现只剩1-1.25%了)和3月11日向市场注资1.5万亿美元,3月13日,国会众议院与白宫达成协议,通过应急法案。至此,政府能做的,货币、财政、行政和立法工作,都做了。其中立法尤其重要,因为行...
|

|
英国 MHRA 关注新冠疫情引发的临床试验相关偏差上升
2020.03.14
英国药品与医疗保健产品监管机构(MHRA)表示,由于新型冠状病毒肺炎(COVID-19)疫情爆发,预计正在开展的临床试验中与试验方案相关的偏差将会增加。世界卫生组织(WHO)于 3 月 11 日宣布 COVID-19 疫情为全球大流行(pandemic)。【WHO 宣布全球大流行,FDA 暂停境外检查和外部会议...
|

|
FDA联手FTC与业界共同商讨如何促进生物类似药竞争
2020.03.13
美国 FDA 和联邦贸易委员会(FTC)于 3 月 9 日举行的生物类似药竞争性市场研讨会吸引了大批与会者参加。会议主要提供了当前生物类似药市场的概况,并给出之前曾再三提出的如何消除生物类似药使用障碍的建议。研讨会大约有 85 人现场参会,另有 300 人通过网络参会。
这是一...
|

|
FDA 发布替代电子格式提交指南,宣布支持新数据标准
2020.03.13
美国 FDA 于3 月 10 日发布《以替代电子格式提交监管申报》的指南草案,详细介绍了有资格获得电子通用技术文档(eCTD)豁免的申报资料的替代电子格式。
上个月 FDA 定稿了《以电子形式申报 — 采用eCTD规范的某些人用药品申请及相关申报资料》,定稿版本是这一指南文件的第七...
|

|
FDA 将于 2021 年新建先进制造实验室促进连续制造...
2020.03.12
美国 FDA 计划于 2021 年在其总部附近建立一座制造研究实验室,以容纳一个用于模拟原料药和制剂制造过程的试验工厂,促进对新型制造技术的评估。根据 FDA 2021 年预算要求文件,其在基础设施建设上的预算要求预计增加 630 万美元,新制造实验室将帮助其推广先进制造技术,例如连续制...
|
|
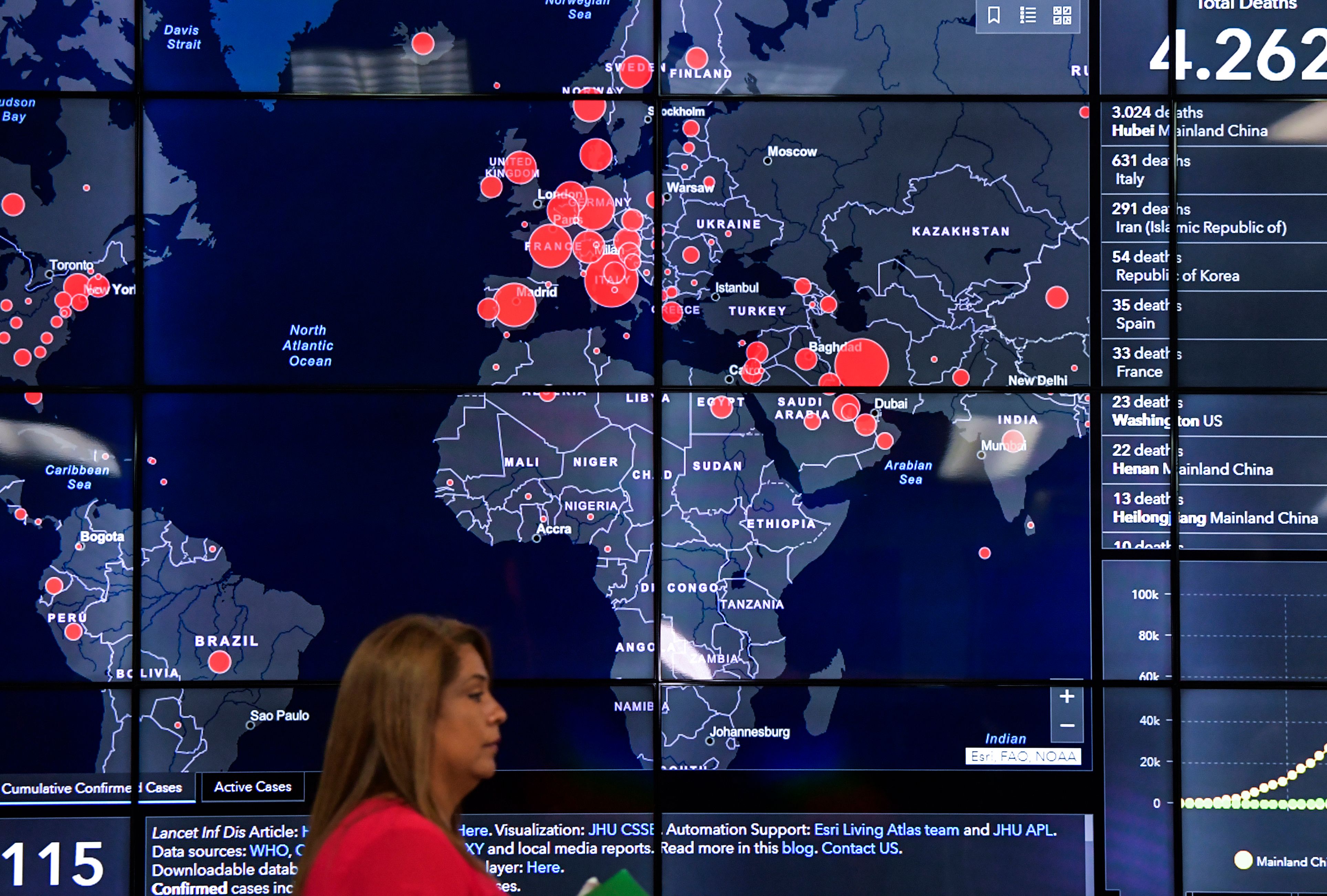
WHO 宣布全球大流行,FDA 暂停境外检查和外部会议
2020.03.12
当地时间 3 月 11 日晚,WHO 总干事谭德塞宣布新型冠状病毒肺炎(COVID-19)疫情为全球大流行(pandemic),并表示情况将进一步恶化。谭德塞表示,“宣布大流行并不会改变 WHO 目前针对新冠肺炎疫情的评估和正在开展的工作。”
WHO 紧急卫生计划负责人 Mike Ryan 在本周一...
|
|
FDA 发布评估 2 型糖尿病治疗药安全性的新指南,不...
2020.03.11
美国 FDA 于 3 月 9 日发布《2 型糖尿病:评估新药的安全性以改善血糖控制》指南草案,倾向于对目标人群的心血管风险评估进行更长期且更广泛的安全性评估。
新指南草案取代了 FDA 2008 年关于评估 2 型糖尿病药物心血管风险的指南以及 2008 年发布的关于开发治疗或预防糖...
|

|
FDA 新发布指南鼓励将老年患者纳入癌症临床试验
2020.03.11
美国 FDA 于 3 月 5 日发布指南草案《在癌症临床试验中纳入老年患者》,希望鼓励制药商在癌症临床试验中纳入更多老年患者,以确保这些研究中的患者人群能够更好地反映真实世界中的患者人群。
FDA 肿瘤卓越中心主任 Richard Pazdur 表示,“在临床试验中招募广泛的患者代表是...
|
|
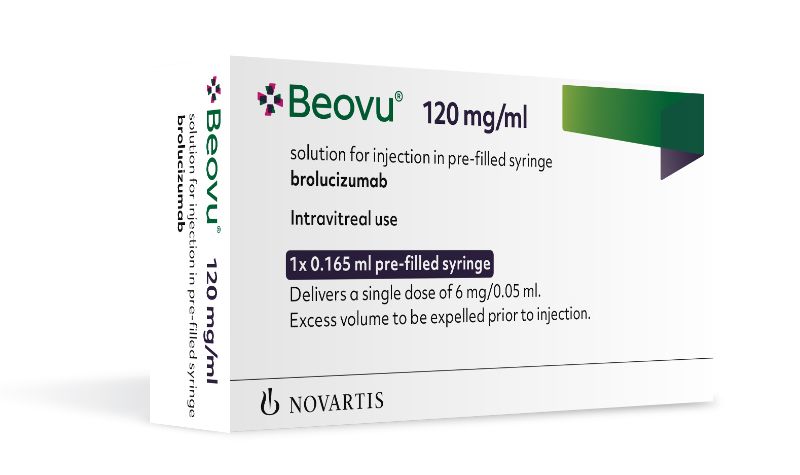
诺华前雇员起诉称因揭露数据错误而被解雇
2020.03.10
诺华公司一名前雇员称她因指出诺华关于眼用药 Beovu 的不正确安全性数据而被开除。
Zuhal Butuner 在去年 2 月份提起的诉讼中描述了她曾在 2018 年 3 月建议诺华就有关 Beovu(brolucizumab)的已发布安全性数据中的“重大错误”发布新闻稿或向医生发信,Beovu 当时是正在...
|

|
最新研究估算药物开发成本约为 13 亿美元,引发各方...
2020.03.10
关于新药开发的成本估算一直以来被用作在药品投放市场后定价辩论中的武器。制药业通常引用 2016 年 Tufts 大学药物开发研究中心的成本研究数据 28 亿美元1,认为价格必须足够高才能弥补巨大的财务风险。但是有批评人士有时会引用低至 4300 万美元的数字,认为较高的药物研发成本只...
|

|
【更新提示】识林一周回顾(20200302-0308)
2020.03.09
上周国家局再次应急审批了1个新型冠状病毒抗体检测试剂盒,发布药品委托生产质量协议指南和上市许可持有人检查工作程序和要点;FDA 发布 33 篇新增和 10 篇修订 BE 指南,识林发布相应花脸稿指南对比;FDA 还发布有关应对新型冠状病毒疫情的更新,包括发布有助于加速诊断面市的新政...
|

|
欧盟专家解读17版无菌附录修订,IPEM-识林疫期学习计...
2020.03.09
2018年IPEM无菌课程,老师说:17版无菌附录增加了很多新兴技术,但没讲清楚还不如不写,比如一次性技术,后来20版这部分加了两条,文字增加了20%
他还说:生物负荷(bioburden)过度强调标准可能走偏了方向,先把房间弄脏,再打扫干净不是好的GMP,应该从源头和整个流程保证无菌。
...
|
|
【周末杂谈】看 FDA 处理 Daraprim 事件
2020.03.08
2月28日,美国FDA批准了艾滋病患者使用的、治疗寄生虫感染的药品Daraprim达拉匹林25毫克(原料药是pyrimethamine,乙胺嘧啶)的第一个仿制药。达拉匹林和其所属图灵(Turing)公司,2015年曾产生了轰动性新闻。图灵总裁Martin Shkreli将药品从每片13.5美元飙升到750美元(5000%),并在...
|
|
药房质疑FDA对二甲双胍中NDMA的检测结果,要求独立第...
2020.03.07
美国一家在线药房倡导制定法规对药品化学成分进行独立检测和核实,并指出 FDA 评估二甲双胍致癌性风险的检测方法需要改进。
Valisure 是美国一家在分发药品之前开展药品检验的在线药房,其于 3 月 2 日提交公民请愿,呼吁 FDA 颁布新规,要求在药品分发到患者手中之前,必须对...
|

|
FDA 最新指南明确排除“授权生物类似药”的存在
2020.03.06
距离某些蛋白质产品从作为药品监管过渡到作为生物制品监管仅剩不到三周的时间【视为许可产品从 NDA 到 BLA 过渡的监管变化】,美国 FDA 于 3 月 4 日发布《生物制品价格竞争与创新法案中“视为许可”条款问答》定稿指南,澄清 3 月23 日之后在竞争激烈的胰岛素领域,哪些类型...
|

|
【文献】色谱法:天然药物研发的重要工具
2020.03.06
2020年1月,来自印度印度科学与工业研究理事会(CSIR)-印度中西医研究所(IIIM)的Alamgir Ahmad Dar博士在《分离科学杂志》(Journal of Separation Science)杂志上发表了一篇名为Chromatography An important tool for drug discovery的综述文章,对色谱分析方法在天然产物(...
|

|
FDA 指南快读(Guidance Snapshots)试点计划一瞥
2020.03.05
美国 FDA 于 2 月 28 日宣布了一项新的试点项目:为一系列与现代化药物临床试验和加速药物开发相关主题的跨领域指南文件发布“指南快读”。
到目前为止 FDA 已经针对其中的三份指南发布了快读,这些快读使用了形象简洁的语言,提供了指南中的重点内容。其中两份快读与通过临床...
|