|
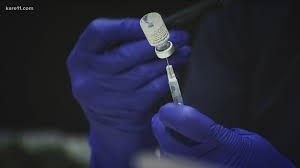
FDA 授权辉瑞新冠加强疫苗,虽有限制适用人群仍然广...
2021.09.24
美国 FDA 于 9 月 22 日发布了针对辉瑞和 BioNTech 的新冠(COVID-19)疫苗加强针的紧急使用授权。FDA 表示,加强针的使用应仅限于 65 岁以上人群,18 至 64 岁严重新冠疾病高危人群以及因为工作而面临更高感染风险的人群,例如医护人员和教师等。
FDA 代理局长 Janet Woo...
|

|
渤健阿尔茨海默药销售远低预期,公司考虑裁员等措施削...
2021.09.24
本月早些时候,渤健(Biogen)高管公开承认,其治疗阿尔茨海默病的 Aduhelm 的推出速度比预期的要慢。私下里,该公司面临的形势比其公开披露的要惨淡得多,迫使渤健考虑削减成本的措施,包括裁员。
截至 9 月 11 日,只有 100 多名阿尔茨海默病患者注射了 Aduhelm,这一数字正...
|

|
FDA 发布质量相关受控函的问答,涵盖仿制药常见 CMC...
2021.09.23
美国 FDA 药品审评与研究中心(CDER)于 9 月 20 日发布了一份题为《质量相关受控函问答》的指南草案为仿制药申请人提供药品质量领域常见问题的解答。新指南旨在对此类问题提供直接答案,以减少有关相同主题的受控函数量。
指南采用问答形式,涵盖了 FDA 关于质量相关科学和监...
|
|
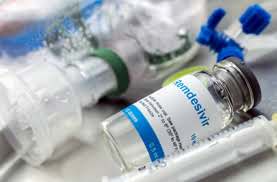
最新研究表明早期使用瑞德西韦可减少新冠住院率
2021.09.23
吉利德(Gilead )于 9 月 22 日表示,其新冠(COVID-19)瑞德西韦(remdesivir)在一项新研究中似乎将在疾病早期诊断出的高危患者的住院率降低了 87%。
吉利德在公司的新闻稿中发布的新结果可能有助于巩固对这种药物有效性的看法,同时还可以提高人们对使用辉瑞和默沙东等制药...
|

|
ICH 调研显示指南实施和采纳水平普遍较高
2021.09.22
根据 9 月 9 日公布的一项最新调研结果显示,ICH 的 55 份与质量、安全性和有效性相关的指南以及多学科指南中的大部分已被其 10 个非创始成员和观察员以及 30 家制药企业采纳。
该调研旨在监测监管机构和行业对 ICH 指南实施的充分性和水平,并补充 2019 年发布的关于 I...
|

|
FDA 发布非处方药商欠款清单,超五百家企业未按时缴...
2021.09.22
美国 FDA 发布了第一份有关未能支付 2021 财年的非处方药专论使用者付费法案(OMUFA)规定的设施费的欠款清单。对于在 2021 年 5 月 10 日到期之前未支付的费用,发票已于 2021 年 6 月 25 日通过电子邮件发送。拖欠名单上有近 500 家公司,其中 28 个是合同制造组织(CM...
|

|
【一周回顾】2021.09.13-09.19
2021.09.20
药审中心发布 CAR-T 产品申报上市临床风险管理计划技术指导,就 ICH E14 指南翻译公开征求意见。美国 FDA 更新生物类似药研发和生物制品价格竞争与创新法案问题与解答指南,新成立数字化转型办公室。美国 FDA 和欧盟 EMA 启动复杂仿制药/混合产品并行科学建议试点计划。
...
|

|
英国政府启动新系统监测临床试验报告披露
2021.09.20
经过长期努力,英国政府现在正在跟踪临床试验申办人是否报告试验结果,这一透明度运动将迫使大学和企业加强结果披露。
此举是在 2018 年的一项分析发现许多试验申办人(其中一些由政府资助)未能报告其研究结果之后做出的【欧洲临床试验信息公开的缺乏所引发的关注 2018/11/15】。...
|

|
【周末杂谈】产品全生命周期的质量风险和经济学
2021.09.19
从质量风险、公众健康和公共财政角度看产品生命周期的药物经济学
IPEM教师、著名仿制药专家Garth Boehm博士曾讲过如下的故事。约30年前,美国仿药企业Purepac年产Hydrochlorothiazide(氢氯噻嗪片,一种保钾利尿剂,25mg规格)70吨,总收入(不是净收入)才80万美元。为了挣这点钱,企...
|
|
【快讯】FDA 新冠疫苗加强针专家会:16-2 反对全员...
2021.09.18
北京时间 9 月 18 日 4 点 40,美国 FDA 就辉瑞新冠 mRNA 疫苗 COMIRNATY 的加强针申请召开的专家会结束。在经历了一整天对新冠疫苗加强针的讨论后,起初专家组投票反对批准辉瑞新冠疫苗的加强针,之后 FDA 修改了问题获得了专家组的一致通过。虽然讨论专门针对辉瑞新冠疫...
|

|
吃了有致癌物的药还要补偿制药商诉讼成本:雷尼替丁仿...
2021.09.17
看了题目大家可能觉得有点稀奇,但事实确实如此。故事还要从两个月前说起,今年 7 月 8 日,美国一名联邦法院法官驳回了针对数十家 Zantac(善胃得,雷尼替丁)仿制药商和零售商所销售的雷尼替丁仿制药可能含有致癌物质的指控【法院驳回对雷尼替丁仿制药商和药房关于亚硝胺杂质致癌风...
|

|
FDA 通过新的数字化转型办公室继续推进数据现代化
2021.09.17
美国 FDA 于 9 月 15 日宣布将其信息技术(IT)、数据管理和网络安全职能改组为新的数字化转型办公室(ODT)。该办公室将直接向 FDA 局长报告,将办公室及其职能提升到整个机构级别。
FDA 表示,此次改组将通过改进数据和 IT 能力推动 FDA 的信息技术转型,从而改善机构运...
|
|
FDA 发布辉瑞新冠疫苗加强接种专家会会前资料,对加...
2021.09.16
根据美国 FDA 9 月 15 日公布的专家会会前资料,FDA 科学家对是否需要为所有接种过辉瑞新冠疫苗的人提供加强夹中表示怀疑。FDA 将于 9 月 17 日召开专家会议就哪些人群需要额外的加强接种以及何时需要加强接种进行辩论。
在文件中,FDA 自己的科学家似乎对广泛使用加强接种...
|

|
FDA 和 EMA 启动复杂仿制药-混合产品并行科学建议...
2021.09.16
美国 FDA 和欧洲药品管理局(EMA)于 9 月 15 日宣布启动了一项试点计划,为 FDA 复杂仿制药产品的简化新药申请(ANDA)和 EMA 混合产品上市许可申请(MAA)的申请人提供并行科学建议(PSA)。该试点项目是 FDA 和 EMA 现有新药和生物制品 PSA 的扩展。
试点计划允许向 FDA ...
|
|
阿尔茨海默实验性新药 simufilam 被质疑数据造假,...
2021.09.15
美国 Cassava 科学公司首席执行官 Remi Barbier 于 9 月 13 日在投资银行 H.C. Wainwright 的投资者会议期间通过预先录制的视频发言表示,其名为 simufilam 的阿尔茨海默实验性治疗药物是安全的,因此 FDA 不应干涉公司启动后期临床试验的计划。Barbier 还声称 Cassav...
|

|
三分之一加速批准的癌症适应症在确证性试验失败后仍保...
2021.09.15
英国医学杂志(BMJ)上发表的一项分析发现,即使在后续研究未能证实获益之后,三分之一获得加速批准的抗癌药的产品标签上仍保留有这些适应症。同时,被广泛阅读的医生指南也在继续推荐这些治疗方法。
这一研究是针对近三十年前创建的加速审批计划,该计划是为了加快医疗需求未得到满足...
|

|
FDA 致信专利局就专利陷阱、产品跳转和专利常青等关...
2021.09.14
美国 FDA 正在寻求与专利商标局(PTO)就各种热点问题进行合作。9 月 10 日,FDA 代理局长 Janet Woodcock 致信美国知识产权商务部副部长兼 PTO 局长 Andrew Hirshfield,寻求从专利审判和上诉委员会(PTAB)到专利期限扩展再到“可能滥用专利制度”的所有方面进行合作。
Wood...
|

|
即将离任的 FDA 疫苗办公室正副主任柳叶刀发文称目...
2021.09.14
美国 FDA 疫苗研究与审评办公室(OVRR)主任和副主任在 9 月 13 日《柳叶刀》发布的一篇文章上表示,即使针对德尔塔变体,疫苗对严重新冠疾病的有效性仍然很高,从而在疫情现阶段对普通人群进行加强接种是不合适的。
这两名领导人 Marion Gruber(OVRR 主任)和 Phil Krause(O...
|

|
【一周回顾】2021.09.06-09.12
2021.09.13
识林发布 2021 年 7-8 月美国和欧盟药品审批情况报告。美国 FDA 启动新型辅料审评试点计划;更新新冠期间简化新药申请的开发问答指南,公布一封 483。英国批准辉瑞和阿斯利康新冠疫苗加强针。欧盟更新亚硝胺杂质 Step 2 模板。
上周热点资讯:
因不卖参照药品引发的官司...
|
|
美国药品追溯跟踪举步维艰:业界呼吁 FDA 撤销电子...
2021.09.13
美国药品分销商敦促 FDA 立即撤销其设定参数用于建立电子系统以在整个供应链内追溯跟踪产品的指南。分销商贸易协会称,FDA 寻求在贸易伙伴之间获取私有电子追踪信息时超出了其法定权力。
FDA 于今年 6 月发布《根据在包装级别增强药品分销安全》指南草案,为构建计划于 2023 年 1...
|