
|
到期一年后,FDA 罕见儿科疾病优先审评券重获生机
2025.09.25
9月17日,美国众议院能源与商业委员会对“给孩子们一个机会法案”(Give Kids A Chance Act)进行了标记修订,该法案旨在重新授权FDA的罕见儿科疾病优先审评券(Rare Pediatric Disease Priority Review Voucher,RPD PRV)计划,并在若干相关领域强化FDA的权力。
RPD PRV计划...
|

|
2026年 FDA 优先审评券费率下调21%,披露优先审评...
2025.09.25
9月18日,FDA通过联邦公告发布通知,正式确定2026财年使用优先审评券(Priority Review Voucher,PRV)的费率为1,962,472美元。该费率自2025年10月1日起生效,有效期至2026年9月30日。
识林读者对PRV并不陌生。这项机制旨在激励企业开发针对热带疾病、罕见儿科疾病及重大威胁公共...
|

|
欧盟变更指南定稿,2026年1月15日正式适用
2025.09.24
9月22日,欧盟委员会(European Commission,EC)发布了最终版《药品变更指南》(Variations Guidelines),明确该指南自2026年1月15日起正式适用。该指南现行版发布于2013年8月,分别在2024年6月和2025年6月两次征求意见。
此前2025年1月1日,欧盟《药品变更法规》(Variations Regul...
|
|
FDA 更新指南,指导药企应对监管要求的说明书安全信...
2025.09.24
9月18日,FDA发布了《安全性标签变更 — FD&C法案第505(o)(4)节的实施》指南草案,旨在指导制药行业实施FD&C法案第505(o)(4)节授权给FDA主动提出的安全性标签变更(SLC)相关要求。现行指南早在2013年发布,从花脸稿对比可知,FDA进行了大面积修订。
FD&C法案第505(o)(4...
|

|
药企与 FDA 交流 CMC 试点计划,工作量增加且吸引...
2025.09.23
9月10日,FDA官员与制药行业代表在一场专题研讨会上就FDA的CMC开发和准备试点(CMC Development and Readiness Pilot,CDRP)计划进行了深入交流。
CDRP计划自2022年10月启动,适用于具有加速临床开发时间框架的NDA和BLA,包括获得突破性疗法、快速通道和再生医学先进疗法认定的...
|

|
英国 MHRA 更新指南,提供与多家国际监管机构的审评...
2025.09.23
9月17日,英国药品和健康产品管理局(MHRA)更新了《国际认可程序》(International Recognition Procedure,IRP)指南。该指南最早于2023年8月发布,自2024年1月1日起正式实施。该程序取代了之前的欧盟委员会决策信赖程序(EC Decision Reliance Procedure,ECDRP),并将互认/分...
|

|
国际药政每周概要:FDA 优先审评券费率,更新2种胃食...
2025.09.23
【早期开发与临床】
9.16,【FDA】侵蚀性食管炎:开发治疗药物(征求意见稿)
9.16,【FDA】症状性非侵蚀性胃食管反流病:开发治疗药物(征求意见稿)
9.16,【FDA】播散性球孢子菌病:开发治疗药物(征求意见稿)
【注册审评】
9.17,【MHRA】国际认可程序(定稿)
9...
|

|
国内药政每周导读:CDE 沟通交流2025版,医保局集采...
2025.09.22
【早期开发与临床】
9.18,【CDE】关于公开征求《用于术后镇痛的长效局部麻醉药临床试验技术指导原则(征求意见稿)》意见的通知
【CMC与仿制药】
9.16,【CDE】关于公开征求《预防用疫苗佐剂药学研究技术指导原则(征求意见稿)》意见的通知
9.16,【CDE】关于公开征求《预...
|

|
CIRS 报告纳入 NMPA,展示国际化新药在中国的获批趋...
2025.09.22
9月16日,国际组织监管科学创新中心(Centre for Innovation in Regulatory Science, CIRS)发布报告《追踪六大全球主要市场已批准药品在中国的上市情况》(CIRS RD Briefing 102–Tracking Availability in China of Medicines Approved in Six Key Global Markets),追...
|

|
BsUFA III 下生物类似药补充申请分类与审评时间线
2025.09.22
9月8日,FDA发布了《BsUFA III下某些补充申请的分类类别》定稿指南,明确了生物类似药六类需预先批准的补充申请(A至F类)的界定标准及相应的审评绩效目标,并给出提交补充申请的具体步骤。
六类补充申请均属于临床变更
现将六类补充申请情形概述如下,供我国出海药企参考。指南...
|

|
【周末杂谈】基于风险做法的初衷
2025.09.21
提倡采用风险评估的做法,就是提倡对产品和工艺的科学认知
当年北京大学国际药物工程管理(IPEM)硕士项目主讲仿制药注册的王建英女士,曾因如下一句话博得学员的尊敬:“这是要求的,但可以不做;那是不要求的,但必须做”。天下恐怕没有药企不拿药品注册当回事。敢如此说和做的人,一定...
|

|
【岗位知识地图】更新18个岗位的法规和知识
2025.09.20
2023年9月,识林推出“中国化学仿制药注册”,“中国化学新药注册”,“原料QA”,“无菌QA”4个常用的岗位知识地图,岗位知识地图模块上线试运行。
运行两年来,岗位知识地图从非临床研究到商业QA,涵盖了药品全生命周期越来越多的环节;从中国到欧盟,从化学仿制药到生物新药,覆盖了越...
|

|
FDA 官方开展的仿制药研究课题概要:药械组合产品
2025.09.19
在《2024财年GDUFA科学与研究报告》中,FDA利用内部资源和外部合作,在九大领域开展了超过70项研究课题,涵盖当前仿制药研发、审评以及监管科学的重大课题,旨在全面促进仿制药产品开发和可及。
如今的仿制药开发已不同以往,在质量和成本的双重压力下,我国仿制药企业有必要迎头赶上...
|

|
【讲座简报】Peter Baker 解读 PICS 与欧盟计算机...
2025.09.19
2025年9月11日,识林邀请了数据可靠性领域专家、前FDA检查员、IPEM项目讲师Peter Baker先生,就PIC/S与欧盟计算机化系统附录的最新修订内容进行了深入解读。本次研讨会重点围绕2025年7月发布的PIC/S 与欧盟新版附录11《计算机化系统》展开,该附录进一步明确了全生命周期管理及基...
|

|
ICH 定稿 M14,协调基于 RWD 的非干预性研究用于...
2025.09.18
9月12日,ICH发布定稿《M14 利用真实世界数据进行药品安全性评价的非干预性研究:规划、设计、分析与报告的总则》。该指南于2024年5月21日进入第2阶段征求意见,2025年9月4日正式采纳进入第4阶段。
指南明确适用范围是针对药品上市后安全性评价的非干预性研究,不涵盖仅依赖国家或地...
|

|
FDA 严厉打击“欺骗性”处方药广告
2025.09.18
9月9日,FDA宣布对直接面向消费者(Direct-to-Consumer, DTC)的“欺骗性”处方药广告实施严厉打击(Crackdown on Deceptive Drug Advertising),计划撤销一项1997年的关键法规,即“充分规定”(adequate provision)要求。该法规目前允许制药企业在广播广告中以简略形式呈现...
|

|
PDA 推出人工智能术语表,厘清制药环境中的 AI 概...
2025.09.17
近日,作为制药业主流技术协会,美国注射剂协会(PDA)为应对人工智能(AI)和机器学习日益突出的重要性,通过其药品制造数字化倡议开发了一套专为制药行业量身定制的独特资源——AI术语表。该术语表提供了清晰、标准化的AI相关术语定义,并增补与药品制造相关的背景信息。
截稿时该...
|

|
FDA 警告信分析揭示 GLP 合规缺陷和经验教训
2025.09.17
近期,有研究者在Journal of Pharmaceutical Innovation期刊发表了一项针对GLP合规的FDA警告信的分析研究,文章题为《药物非临床研究质量管理规范在临床前的研究:从2019年至2024年违反21 CFR Part 58发出的警告信中总结的经验教训》(Good Laboratory Practice in Preclinical Resea...
|
|
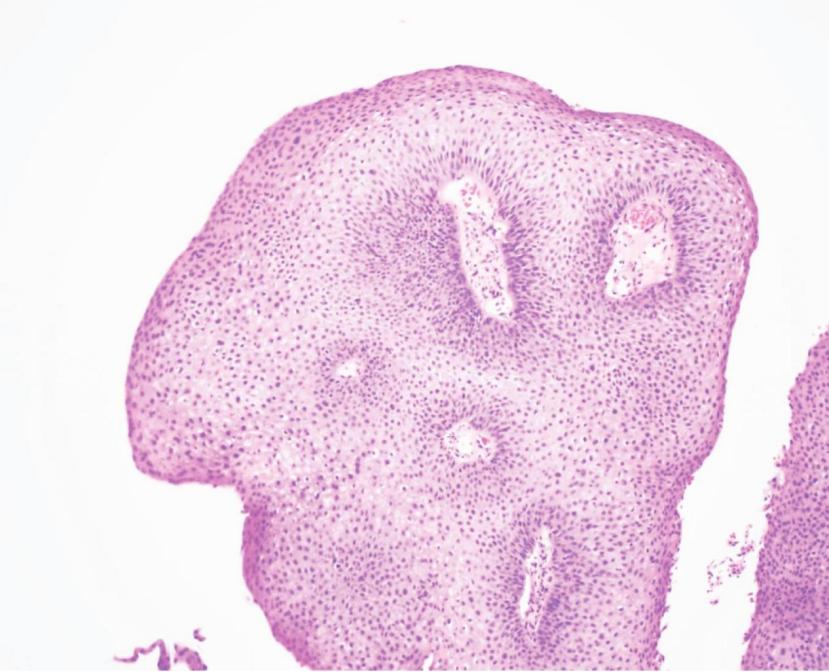
FDA 批准 Papzimeos:单臂试验支持罕见病药物完全批...
2025.09.16
FDA于8月14日批准了Papzimeos(zopapogene imadenovec-drba),成为美国首个用于治疗复发性呼吸道乳头状瘤病(Recurrent Respiratory Papillomatosis,RRP)的疗法。申办方Precigen曾在2023年8月宣布获得FDA的同意将1/2期研究作为单个关键试验,利用人乳头瘤病毒(HPV)特异性免疫...
|

|
批准前检查有望变革,FDA 发布替代工具最终指南
2025.09.16
9月11日,FDA定稿《替代工具:评估待审申请中确定的药品生产设施》。该指南适用于新药申请(NDA)、简化新药申请(ANDA)、生物制品许可申请(BLA)或这些申请的补充申请,但不适用于批准后检查、常规检查、跟进检查(follow-up)、有因检查和生物研究监测检查(BIMO)。
指南中提到...
|