
|
FDA 紧急修订:临床暂停时仍可认定再生医学先进疗法
2026.03.23
3月12日,FDA生物制品审评与研究中心(CBER)对《SOPP 8215:再生医学先进治疗产品的管理:认定申请、申办者沟通和状态评估》进行了修订,距离上一版本发布(1月9日)仅间隔两个月。
此次修订改动内容有限,但显著改变了FDA对再生医学先进疗法(Regenerative Medicine Advanced Thera...
|
|
FDA 定稿局部用药 Q3 指南,划分三个对比层次
2026.03.23
3月16日,FDA定稿《ANDA 提交的局部用药的物理化学和结构(Q3)表征》指南,与2022年征求意见稿相比并无显著改动。该指南旨在为仿制药申请人提供关于皮肤用(包括皮肤及黏膜)液体和/或其他半固体制剂的物理化学及结构(Q3)特性研究的建议。
该指南的核心在于指导申请人如何开展Q3...
|

|
国内药政每周导读:肿瘤药基于后线的前线研究,全合成...
2026.03.23
【非临床和临床研究】
3.17,【CDE】关于公开征求《抗肿瘤药物基于后线研究数据开展前线适应症临床试验技术指导原则(征求意见稿)》意见的通知
3.17,【CDE】国家药监局药审中心关于发布《新生儿和低龄儿剂量推断技术指导原则》的通告(2026年第25号)
【注册与变更】
3.16...
|

|
【周末杂谈】被收购小公司里程碑款的风险
2026.03.22
这是一桩发生在医疗器械领域的民事案子,对制药业应有借鉴性。
Auris Health曾是300人左右的机器人辅助手术器械研制公司。强生是10余万人的综合药械和健康产品公司。2017年5月,强生发现自研的机器人辅助手术器械落后,遂向竞争对手Auris投资4500万美元。2019年4月强生收购Auris:首付款3...
|

|
【轻松一刻】今天,你养龙虾了吗?
2026.03.21
忽然满城都在养“龙虾”,
代码堆砌甲壳,
算力驱动筋肉,
AI长出了Claw。
只要你一声令下,
它就自顾自,一通抓。
有时抓到些东西,
有时砸碎些东西,
有时还可能夹走你的宝贝——
消失在数字汪洋里
但到头来,
没打磨好场景和流程,
Claw只能...
|

|
罕见病患者团体在 FDA 总部前举行“葬礼”示威
2026.03.20
3月18日,超过100名罕见病倡导者、患者家属及护理人员在华盛顿特区举行示威活动。他们首先将一具象征性的棺材运送至FDA总部,随后游行至国会山。此次活动旨在抗议FDA因监管延迟,导致黏多糖贮积症(MPS)患者可能失去治疗机会。
根据国家MPS协会发布的声明,当天的游行者身穿黑衣,在F...
|
|
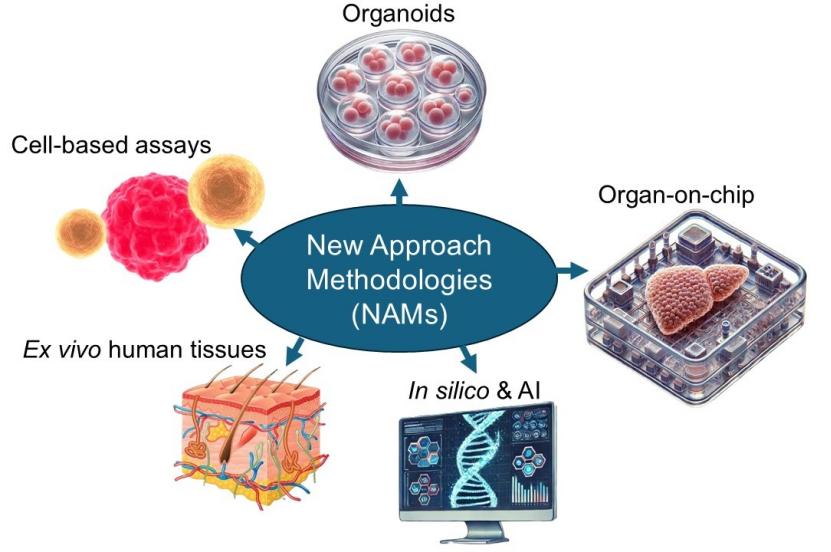
FDA 确立 NAM 验证框架,为动物试验替代打通路径
2026.03.20
3月18日,FDA发布《药物开发中使用新方法学的一般考虑》行业指南草案。该指南旨在为药物研发者提供一个关于新方法学(New Approach Methodologies, NAM)的验证框架,进而优化对人体毒性的预测,并逐步减少对动物试验的依赖。
该指南是FDA继2025年12月简化单抗药物非临床研究之后...
|

|
FDA 局长拟大幅改革 IRB,应对中国临床启动速度挑战
2026.03.19
FDA局长Marty Makary近日在多个公开场合阐述了其对美国临床试验监管体系,特别是机构审查委员会(Institutional Review Board,IRB)运作流程的改革主张,其言论直指美国在新药早期研发阶段与中国相比正在丧失竞争力。
在2026年3月于巴尔的摩举行的美国医疗保险和医疗补助服务中心(...
|

|
PDUFA VIII 谈判动态:资金需用于审评人员,“美国...
2026.03.19
*截图自识林页面。会员可点击查阅最近更新的PDUFA VIII谈判会议纪要。
随着现行《处方药用户付费法案》(PDUFA VII)将于2027年9月到期,其下一迭代版本PDUFA VIII的重新授权谈判自2025年底启动以来,FDA与制药行业已通过一系列会议就多项关键议题进行了深入探讨。近期公布的系列...
|

|
EMA 简化先进治疗药品 OOS 批次使用
2026.03.18
3月3日,EMA发布更新版《已获批的基于细胞/组织的先进治疗药品的超标批次使用问答》,该文件基于2019年6月版本修订。
文件以五个问答形式,明确了已获批上市先进治疗药品(ATMP)在发生超标(OOS)批次时的使用条件、通知程序、记录保存及患者告知等环节的具体要求。主要更新是简化向E...
|
|
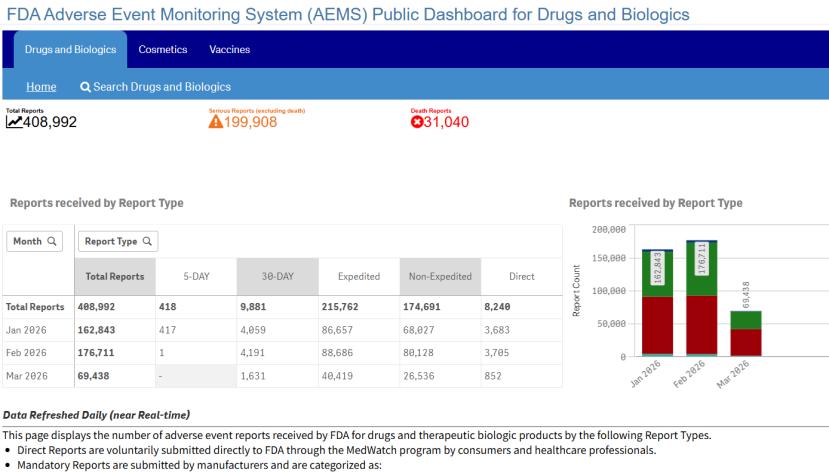
FDA 用 AEMS 整合 FAERS 等全部7个不良反应报告...
2026.03.18
3月11日,FDA宣布启动新的不良事件监测系统(Adverse Event Monitoring System,AEMS)。该平台将整合FDA原有的七个不良反应报告数据库,解决此前系统分散、数据访问困难的问题。这是FDA局长Marty Makary“激进透明”政策在2025年公开完全回应函(CRL)和实时公开不良反应报告数据之...
|
|
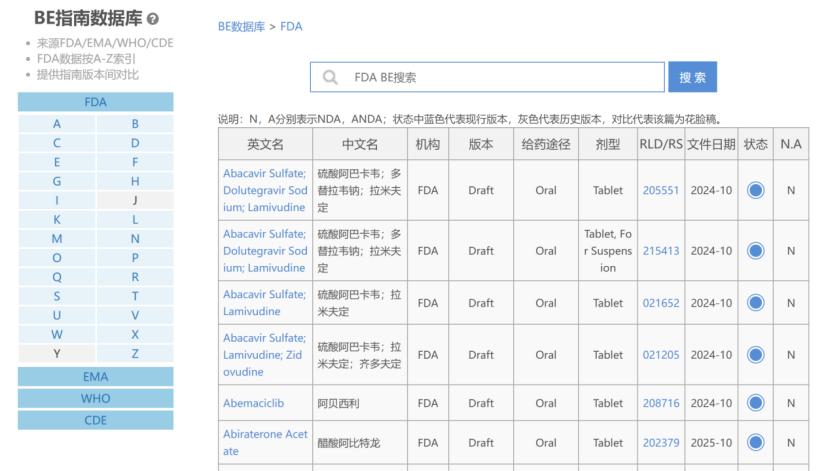
FDA 发布98份 BE 指南,包含多个国内有参比无指南...
2026.03.17
2月26日,FDA发布了98份药品特定指南(PSG)草案,包括31份新指南和67份修订指南。68份PSG针对尚无获批ANDA的药品(包括31份复杂药品),46份PSG针对复杂药品(包含7份新增和39份修订)。
Lachman的仿制药专家Pollock指出值得关注的PSG包括:
用于治疗阿片类药物使用障碍的丁丙诺...
|

|
FDA 兑现亚叶酸钙片“老药新用”,但并非自闭症特效...
2026.03.17
3月10日,FDA批准了已过专利期的药物亚叶酸钙片(leucovorin calcium)用于治疗特定类型的脑叶酸缺乏症。该批准并非基于新的临床试验数据,而是依赖于对现有文献和自然史数据的系统回顾。
此次适应症扩展针对的是由FOLR1基因突变引起的遗传性脑叶酸转运缺乏症(cerebral folate transp...
|

|
国际药政每周概要:FDA 减免生物类似药桥接试验,整...
2026.03.17
【非临床与临床研究】
3.13,【EMA】关于制定支持儿童患者抗癌药品开发的概念验证数据的思考性文件的概念性文件
【药学研究】
3.9,【FDA】生物类似药研发和生物制品价格竞争与创新法案问题与解答 新增和修订内容草案
3.13,【EMA】附录1:N-亚硝胺的可接受摄入量:更新...
|

|
从把关到引导,EMA 对拥有丰富管线的大药企开放新沟...
2026.03.16
3月10日,EMA发布通知,邀请拥有丰富管线(large portfolio)的大型药企申请于2026年下半年举行的产品组合和技术会议(Portfolio and Technology Meeting,PTM)。本次申请的截止日期为2026年4月30日。
PTM是EMA面向创新药研发企业提供的一种专项沟通机制,旨在识别影响产品管线...
|

|
EMA 筹划2026-2028年欧盟药品 AI 监管和内部应用
2026.03.16
3月9日,EMA发布了《NDSG 2026-2028年工作计划:药品监管中的数据与AI》,规划欧洲药品监管网络(EMRN)未来三年在数据与人工智能(AI)领域的关键行动,以应对技术变革,提升监管效能。
文件围绕战略与治理、数据分析、AI、数据互操作性、利益相关方参与及变革管理、指南与国际合...
|

|
国内药政每周导读:HPV 和流感疫苗临床,ADC、生物类...
2026.03.16
【非临床和临床研究】
3.11,【CDE】关于发布《人乳头瘤病毒疫苗临床试验技术指导原则(修订版)》的通告(2026年第23号)
3.11,【CDE】关于发布《流感病毒疫苗临床试验技术指导原则(试行)》的通告(2026年第24号)
【药学研究】
3.9,【NMPA】关于发布仿制药参比制剂...
|

|
【周末杂谈】降低临床试验要求,节省研发成本,对谁不...
2026.03.15
FDA单一关键性临床试验的良策,似乎并未引起产业的欢呼雀跃,为何?
上月,FDA局长Marty Makary和生物中心(CBER)主任Vinay Prasad(已确定4月底离职)联名在《新英格兰医学杂志》上撰文,宣布未来FDA的新药审批多数只需基于一项关键性临床试验。这项为企业降低研发成本的良策,发表近...
|

|
【主题词】人工智能,贝叶斯方法,eCTD,委托生产,互...
2026.03.14
主题词,是识林针对制药行业的关键概念,基于大量资料的综合分析,从定义、工作流程、法规指南、文献案例等多个维度梳理的系统知识纲要。截至目前,识林【主题词库】已上线超过1000个主题词。
从主题词入手,也是使用识林的最佳方式之一。主题词的系统性、全面性和索引功能,既适合岗位...
|

|
【翻译】FDA 新药报告,生物类似药减免临床指南,立...
2026.03.14
中外法规指南浩如烟海,为帮助用户跨越语言关,加深理解,识林将努力为识林企业用户提供法规指南翻译,并尽我们所能确保质量。
专业水平所限,差错难免,也希望企业用户在阅读学习的同时,在页面评论区提问、纠偏,企业用户还可联系我们提出法规翻译需求。
此外,对于英文法规指南和...
|